Cải thiện việc kiểm soát PRRS thông qua kiểm soát sự tiến triển của bệnh tiêu hóa
14-Th8-2023 (Trước đó 1 năm 7 tháng 15 ngày)
Sự xuất hiện của các chủng vi rút PRRS mới cùng với những hạn chế trong việc sử dụng kháng sinh đang làm thay đổi mô hình chăn nuôi heo. Trên khắp Tây Ban Nha, có một thực tế là tỷ lệ tử vong của heo từ lúc cai sữa đến khi xuất chuồng đã tăng 4% do các vấn đề về sức khỏe gia tăng. Mỗi ngày, chúng ta tìm hiểu về các công cụ mới để theo dõi nhiều bệnh lý ảnh hưởng đến trang trại, nhưng chúng ta phải có cách tiếp cận khác biệt so với những vấn đề thông thường và đây là nhiệm vụ của bác sĩ thú y phụ trách: biết cách thay đổi. Để làm được điều này, chúng ta phải dựa vào nghiên cứu mới (sách, bài báo khoa học, v.v.) cũng như trên chính đàn heo.
Hiện đã có tài liệu chứng minh rằng hệ vi sinh vật đường ruột ảnh hưởng rõ rệt đến việc điều chỉnh các phản ứng viêm và do đó, bất kỳ sự rối loạn tiêu hóa nào dẫn đến thay đổi hệ vi sinh vật đều có thể gây giảm đại thực bào phế nang và thay đổi các tế bào đáp ứng miễn dịch Th1 và Th2 (T Helper Leukocytes). Kết quả là, có thể có sự gia tăng phản ứng viêm ở cấp độ phổi cũng như tăng sự tái phát và dai dẳng của các bệnh trên phổi.
Ca bệnh lâm sàng
Chúng tôi đang làm việc với một trang trại có khoảng 2.000 nái đẻ tại vùng Murcia của Tây Ban Nha. Diện tích trang trại khoảng 100 ha, vì vậy các chuồng nuôi heo ở những giai đoạn khác nhau được đặt cách xa nhau. Heo nái sinh sản được nuôi tại một nơi, chuồng cai sữa cách xa khoảng 1 km và chuồng vỗ béo được bố trí cách chuồng nái sinh sản khoảng 3 km.
Trại nái sinh sản dương tính với vi rút PRRS và hiện đang ổn định. Trại có một kế hoạch giám sát hàng tháng bao gồm thu thập các mẫu đầu lưỡi từ heo con chết lưu, phân biệt giữa heo con của nái đẻ nhiều lứa và heo con của nái đẻ lần đầu. Quá trình giám sát này bao gồm xét nghiệm PCR đối với PRRS và PCV-2, với mục tiêu kiểm soát cả hai loại vi rút trong trang trại. Trong giai đoạn này, các phân tích của mẫu đầu lưỡi từ heo chết lưu âm tính với PRRS và PCV-2. Khi một mẫu dương tính với vi rút PRRS, chúng tôi thực hiện giải trình tự bằng ORF5 để kiểm tra xem đó có phải là một chủng mới đến từ sự xâm nhập của vi rút từ bên ngoài hay không. Điều này sẽ cho thấy sự thất bại trong an toàn sinh học bên ngoài.
Trang trại dương tính với Brachyspira hyodysenteriae, nhưng thông qua việc sử dụng vắc-xin tự sinh, các dấu hiệu lâm sàng được kiểm soát và không có triệu chứng nào được quan sát thấy trên heo nái sinh sản hoặc heo nái hậu bị thay đàn đã được tiêm vắc-xin tự sinh nói trên trong kế hoạch tiêm phòng. Bệnh lâm sàng được coi là đã được kiểm soát, mặc dù đôi khi các triệu chứng tương ứng với bệnh kiết lị xuất hiện ở chuồng vỗ béo khi heo nặng khoảng 50-80 kg, đồng thời mất khả năng miễn dịch được truyền từ heo mẹ.
Hiện tượng cắn đuôi ở một mức độ nhất định được quan sát thấy khi xuất chuồng, chúng tôi coi đây là dấu hiệu cho thấy sự hiện diện của bệnh kiết lỵ ngay cả trong trường hợp không quan sát thấy hình ảnh lâm sàng rõ ràng. Nếu heo mắc bệnh cận lâm sàng và do đó bị viêm ruột già, khiến cho chúng có xu hướng trở nên bồn chồn và liên tục cử động đuôi. Như chúng ta đã biết, điều này giống như một cục nam châm thu hút những heo con cùng chuồng của chúng bắt đầu cắn nhau. Một khi hành vi bất thường được thiết lập thì rất khó kiểm soát, vì tình trạng viêm mãn tính gây ra hành vi giống như lo lắng.
Khởi đầu của vấn đề
Các con vật được chuyển đến chuồng vỗ béo với sức chứa 6.000 con được nhập đầy trong bốn tuần liên tiếp. Một tháng sau khi nhập đàn, heo bắt đầu có các dấu hiệu lâm sàng về hô hấp như khó thở dữ dội và chán ăn. Quyết định được đưa ra là áp dụng phương pháp điều trị bằng kháng sinh với florfenicol hòa tan trong nước uống (kết hợp với thuốc chống viêm vào ngày đầu tiên để tăng lượng nước tiêu thụ), nhưng sau liệu trình này, heo vẫn tiếp tục bị chết và không có sự cải thiện nào. Phổi của heo chết có diện tích phổi đông đặc lớn được gửi đến phòng thí nghiệm. Quyết định được đưa ra là áp dụng phương pháp điều trị bằng kháng sinh dạng tiêm (Marbofloxacin) cho toàn đàn, một mặt, ý tưởng là để đảm bảo rằng mỗi con vật nhận được liều lượng thích hợp và mặt khác, đạt được nồng độ kháng sinh hiệu quả trong phổi. Mặc dù tình trạng chung của động vật đã được cải thiện, nhưng sau hai tuần, vẫn quan sát thấy tình trạng tái phát và vẫn không thể kiểm soát được những thiệt hại xảy ra. Hình ảnh lâm sàng trở lại với cường độ như cũ và tiếp tục khiến nhiều heo bị chết (Ảnh 2 và 3).


Các mẫu phổi từ heo chết được gửi đến phòng thí nghiệm và yêu cầu tiến hành xét nghiệm PCR đối với PRRS, PCV-2 và Cúm A. Tất cả các mẫu đều âm tính với PCV-2 và Cúm A và dương tính với vi rút PRRS, vì vậy chúng tôi đã tiến hành giải trình tự virus bằng ORF5 để xem liệu có phải một chủng có độc lực cao đã xâm nhập vào trang trại hay không để có thể giải thích mức độ nghiêm trọng của các triệu chứng lâm sàng này.
Bảng 1. Phân tích mẫu phổi và dịch miệng được lấy tại chuồng vỗ béo.
| Ngày | Chuồng vỗ béo | Mẫu | PRRSv | PCV-2 | Cúm A |
|---|---|---|---|---|---|
| 22/11 | A | Phổi | PRRSv (Ct 28) | - | - |
| 22/11 | B | Phổi | PRSSv (Ct 20) | - | - |
| 22/11 | C | Dịch miệng | PRRSv (Ct 30) | - | - |
| 22/11 | D | Dịch miệng | PRRSv (Ct 36) | - | - |
Tuy nhiên, một mối lo ngại lớn đã xuất hiện: thông thường, khi một mầm bệnh mới xâm nhập vào, nếu nó có tỷ lệ lưu hành thấp thì sẽ tạo ra các triệu chứng lâm sàng vào cuối giai đoạn xuất chuồng và khi tỷ lệ lưu hành của nó tăng lên, các triệu chứng sẽ xảy ra ở heo nhỏ hơn. Tuy nhiên, đây không phải là những gì đã xảy ra trong tháp chăn nuôi này, vì vậy chúng tôi nghĩ rằng việc điều trị bằng kháng sinh sẽ làm giảm tác động của bệnh, nhưng điều này đã không xảy ra.
Khi có được kết quả giải trình tự vi rút PRRS, nó được phát hiện là cùng một chủng vì có sự tương đồng với chủng đang tồn tại trong hệ thống chăn nuôi. Tuy nhiên, nó chưa bao giờ xảy ra theo cách này trong giai đoạn xuất chuồng. Trước đây, các triệu chứng hô hấp đã xuất hiện, nhưng nó dễ dàng được kiểm soát bằng việc sử dụng kháng sinh để điều trị (florfenicol).
Điều gì đã xảy ra với những con heo xuất chuồng có thể giải thích cho sự bất thường này?
Tại thời điểm này, một phương pháp tiếp cận nhiễm trùng mới đang được đề xuất, vì kiến thức ngày càng tăng về trục ruột-phổi và người ta nhận ra rằng những gì xảy ra trong ruột ảnh hưởng đến mức độ nghiêm trọng của bệnh đường hô hấp.
Chúng tôi tự hỏi liệu có bất kỳ bệnh lý nào khác không phải ở phổi mà là ở đường ruột hay không và chúng tôi đã phân lập được Brachyspira hyodesenteriae trong phân. Phát hiện này không phải là mới, nhưng chúng tôi nghĩ rằng nó đã được kiểm soát vì các triệu chứng điển hình của bệnh tiêu chảy xuất huyết niêm mạc không xuất hiện mà chỉ có một số phân mềm, lỏng dường như không có nhiều ý nghĩa lâm sàng.
Liệu sự hiện diện của Brachyspira hyodesenteriae có phải là một trong những nguyên nhân gây ra mức độ nghiêm trọng và dai dẳng của các triệu chứng lâm sàng hay không?
GIẢ THUYẾT: "Sự hiện diện của Brachyspira hyodesenteriae và tác động của nó đối với hệ vi sinh vật đường ruột có thể ảnh hưởng đến quá trình điều tiết các phản ứng viêm với sự gia tăng phản ứng viêm ở cấp độ phổi, đồng thời làm giảm đại thực bào phế nang và do đó tạo ra một môi trường miễn dịch trong đó không thể loại bỏ vi rút PRRS một cách hiệu quả và cũng dẫn đến sự gia tăng tái phát và kéo dài các bệnh trên phổi."
Chúng tôi đã tiến hành xác minh rằng chủng Brachyspira hyodesenteriae đã phân lập vẫn là chủng đang tồn tại trong trang trại và xác định nồng độ ức chế tối thiểu (MIC) cho các loại kháng sinh khác nhau mà chúng tôi phải sử dụng để kiểm soát nó.
Bảng 2. MIC của các loại kháng sinh khác nhau đối với chủng Brachyspira hyodesenteriae được phân lập.
| Chủng SV22-3448 | |||||
|---|---|---|---|---|---|
| Phạm vi kháng sinh thử nghiệm (μg/ml) |
MIC (μg/ml) |
Giải thích độ nhạy | Phạm vi (μg/ml) | ||
| Tiamulin (0.063 - 8) | 0.5 | Trung bình |
≤ 0.25 > 0.25 - ≤ 2 > 2 |
Nhạy cảm Trung bình Kháng |
La và cộng sự, 2016 |
| Valnemulin (0.031 - 4) | < 0.031 | Nhạy cảm |
≤ 0.25 > 0.25 - ≤ 2 > 2 |
Nhạy cảm Trung bình Kháng |
La và cộng sự, 2016 |
| Tylvalosin (0.25 - 32) | 8 | Trung bình |
≤ 0.25 - < 1.5 > 1.5 - ≤ 36 > 36 |
Nhạy cảm Trung bình Kháng |
Pringle và cộng sự, 2012 |
| Lincomycin (0.5 - 64) | 32 | Trung bình |
≤ 4 > 4 - ≤ 36 > 36 |
Nhạy cảm Trung bình Kháng |
Kirchgässner và cộng sự, 2016 |
| Tylosin (2 - 128) | > 128 | Kháng |
≤ 1 > 1 - ≤ 4 > 4 |
Nhạy cảm Trung bình Kháng |
La và cộng sự, 2016 |
Như chúng ta có thể thấy trong Bảng 2, tiamulin dường như là lựa chọn tốt nhất, nhưng ở cấp độ trang trại, khi xem xét các đặc tính vật lý của nước ở vùng Murcia (chất lượng kém và độ mặn cao), loại kháng sinh này sẽ không mang lại hiệu quả tốt, khiến lincomycin có chứa thành phần hoạt chất cung cấp độ bao phủ lớn hơn có thể giải quyết vấn đề lâm sàng tốt hơn. Chúng tôi tiến hành xây dựng phác đồ điều trị bằng kháng sinh tập trung chủ yếu vào việc kiểm soát bệnh lỵ ở cấp độ cận lâm sàng. 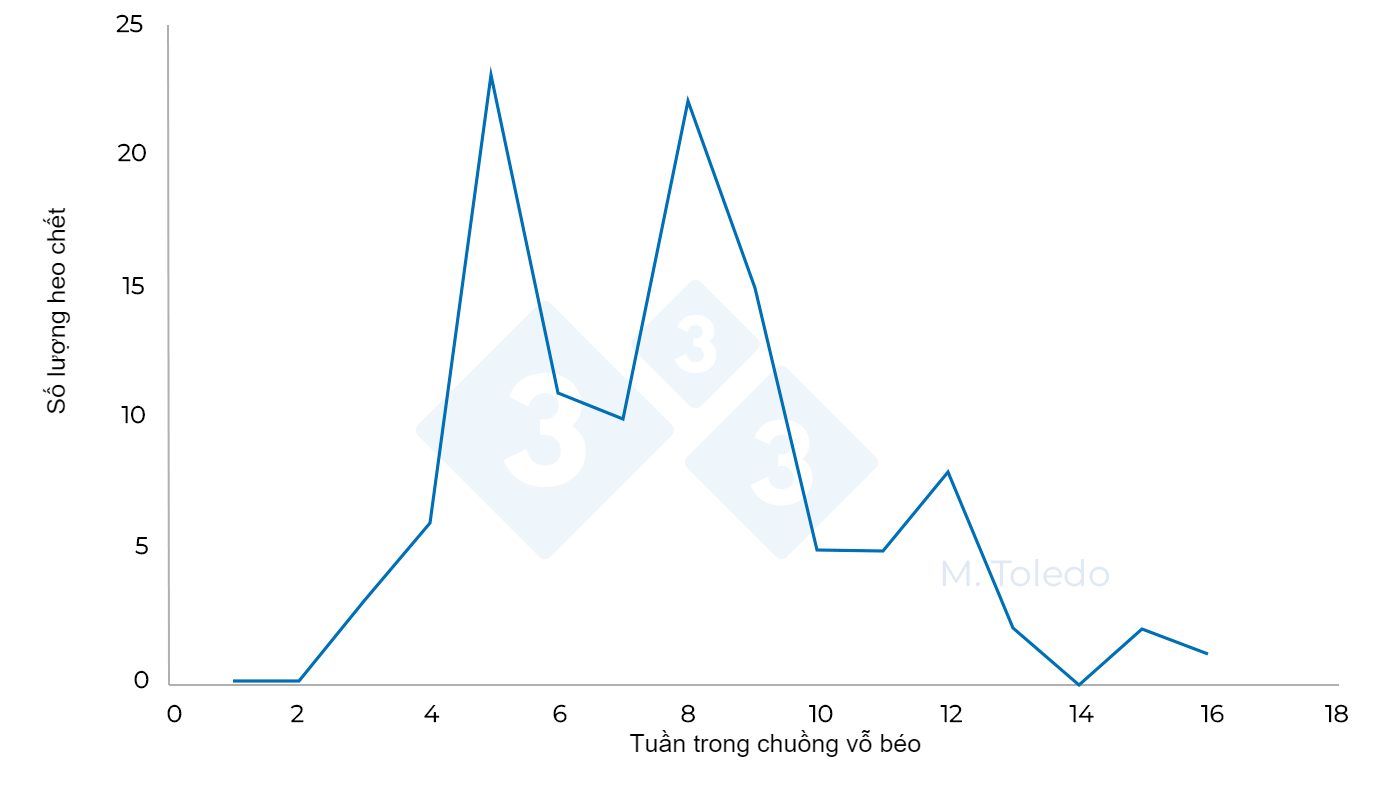
Kết luận
Cách tiếp cận thành công đối với trường hợp lâm sàng này là kiểm soát bệnh kiết lỵ, ngay cả khi chúng tôi phát hiện ra nó ở mức cận lâm sàng. Bằng cách này, bệnh hô hấp tiến triển theo cách ít nghiêm trọng hơn nhiều và không tái phát. Kiểm soát bệnh kiết lỵ cũng dẫn đến giảm sự xuất hiện của các đợt cắn đuôi mới.
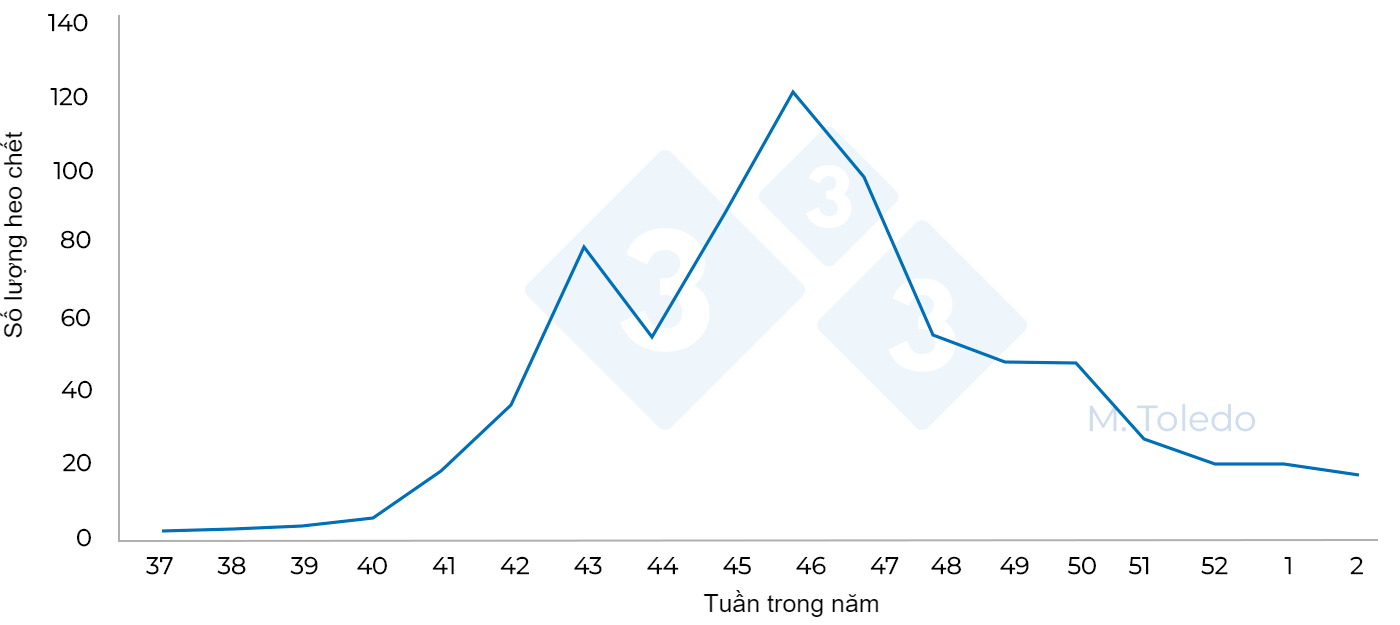
Chúng ta phải bắt đầu tiếp cận các bệnh đường hô hấp theo cách khác (đặc biệt là bệnh gây ra nhiều vấn đề nhất cho chúng ta, vi rút PRRS), bằng cách theo dõi và kiểm soát các rối loạn đường ruột xuất hiện do sự tương tác giữa các mầm bệnh đường ruột khác nhau có khả năng gây ra chứng loạn khuẩn. Điều quan trọng là không xem xét riêng lẻ các tác nhân gây bệnh đường tiêu hóa này vì có nhiều tương tác giữa chúng (Brachyspira spp, Lawsonia intracellularis, Escherichia coli, v.v.). Sự thay đổi này của hệ thống đường ruột có thể điều chỉnh cường độ và thời gian của các bệnh đường hô hấp và do đó, làm phức tạp thêm việc kiểm soát chúng.
