Diagnóstico de PPA - Más que leer los resultados del laboratorio
18-ene-2022 (hace 4 años 2 meses 1 días)
La peste porcina africana (PPA) es una enfermedad viral grave que afecta a cerdos de todas las edades. En los últimos años ha devastado la industria porcina en muchos países. En realidad, la PPA se propaga con bastante lentitud y es posible reducir su avance geográfico mediante acciones apropiadas. Un diagnóstico definitivo y precoz es un elemento clave para evitar su propagación. Se puede realizar un diagnóstico de campo inicial de la PPA a partir de los signos clínicos y los hallazgos de la necropsia.
Signos clínicos:
En la fase inicial de la enfermedad, a menudo se encuentran animales muertos de forma hiperaguda, con cianosis en las patas, orejas y las extremidades. A menudo hay fiebre alta (40 - 42°C); vómitos; diarrea, que puede ser sanguinolenta o negra (foto 1, derecha); depresión; abortos (foto 1, izquierda); secreción nasal sanguinolenta (epistaxis) y aumento de las pérdidas por mortalidad.
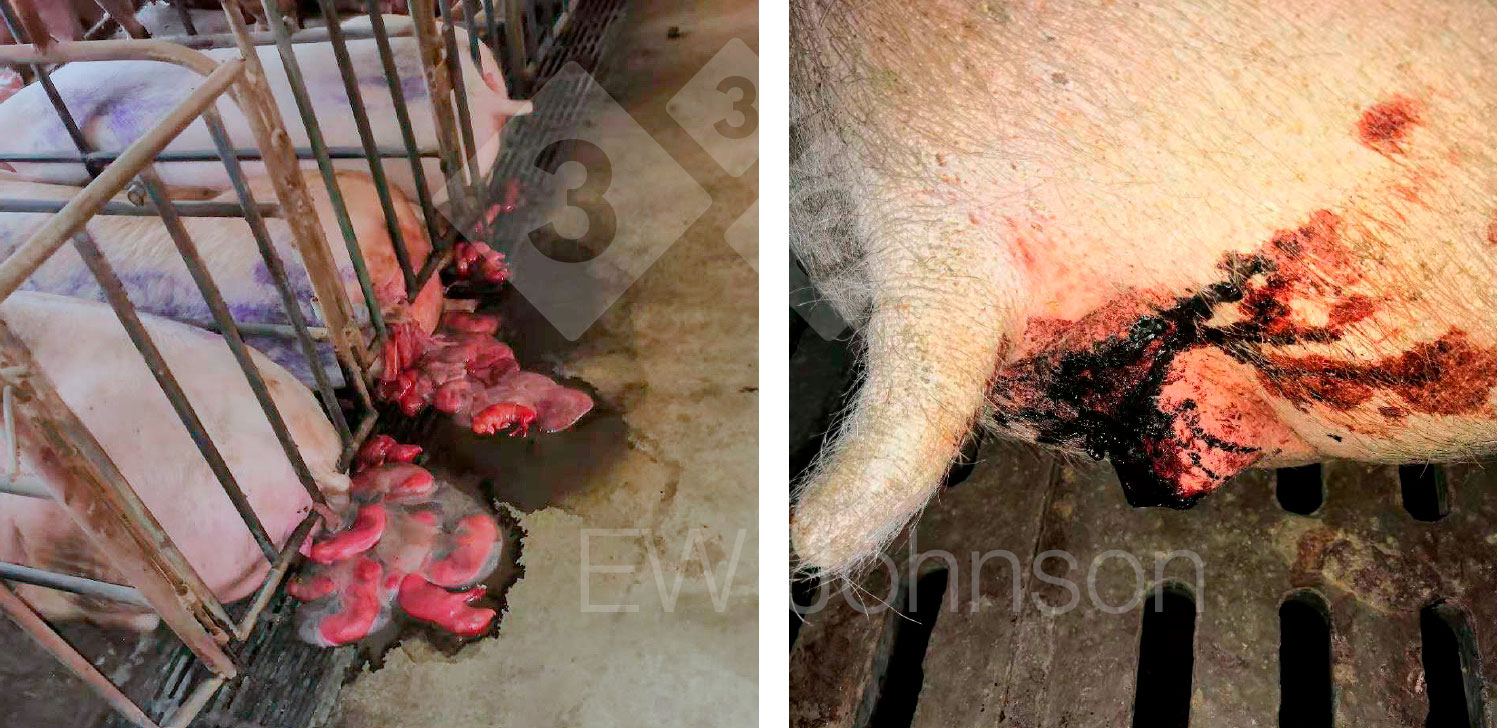
Las cepas poco virulentas (o vacunales) causan una forma atípica leve y crónica de la enfermedad, con pocas muertes. Las hembras suelen mostrar enfermedad respiratoria crónica e infertilidad crónica. El proceso más largo hasta mostrar evidencias de enfermedad, o la falta de signos clínicos observados en los cerdos con el virus vacunal cronificado, se interpreta a menudo en la granja como un largo período de incubación.
Lesiones en la necropsia
- La epiglotis y la tráquea pueden estar enrojecidas y, generalmente, hay una neumonía intersticial con edema interlobulillar. A veces hay pleuroneumonía fibronecrótica que recuerda a App.
- Puede haber miocarditis fibrinosa y pericarditis y el tórax y el abdomen pueden tener un exceso de fluido sanguinolento o serosanguinolento.
- Los linfonodos mesentéricos y, en especial, los gastrohepáticos pueden estar agrandados, edematosos y con apariencia necrohemorrágica al corte (foto 2).
- El bazo puede estar agrandado, con múltiples infartos o puede ser básicamente normal.
- A menudo el hígado tiene hemorragias manifiestas.
- Los riñones pueden tener numerosos infartos y hemorragias petequiales y equimóticas (foto 3). Puede haber un edema perirrenal llamativo. El estómago fúndico suele estar severamente erosionado y el colon espiral puede estar lleno de un contenido sanguinolento. No es raro encontrar hemorragias con aspecto de pinceladas en las vísceras abdominales.
- Puede ser evidente una meningitis fibrinosa en el cerebro.
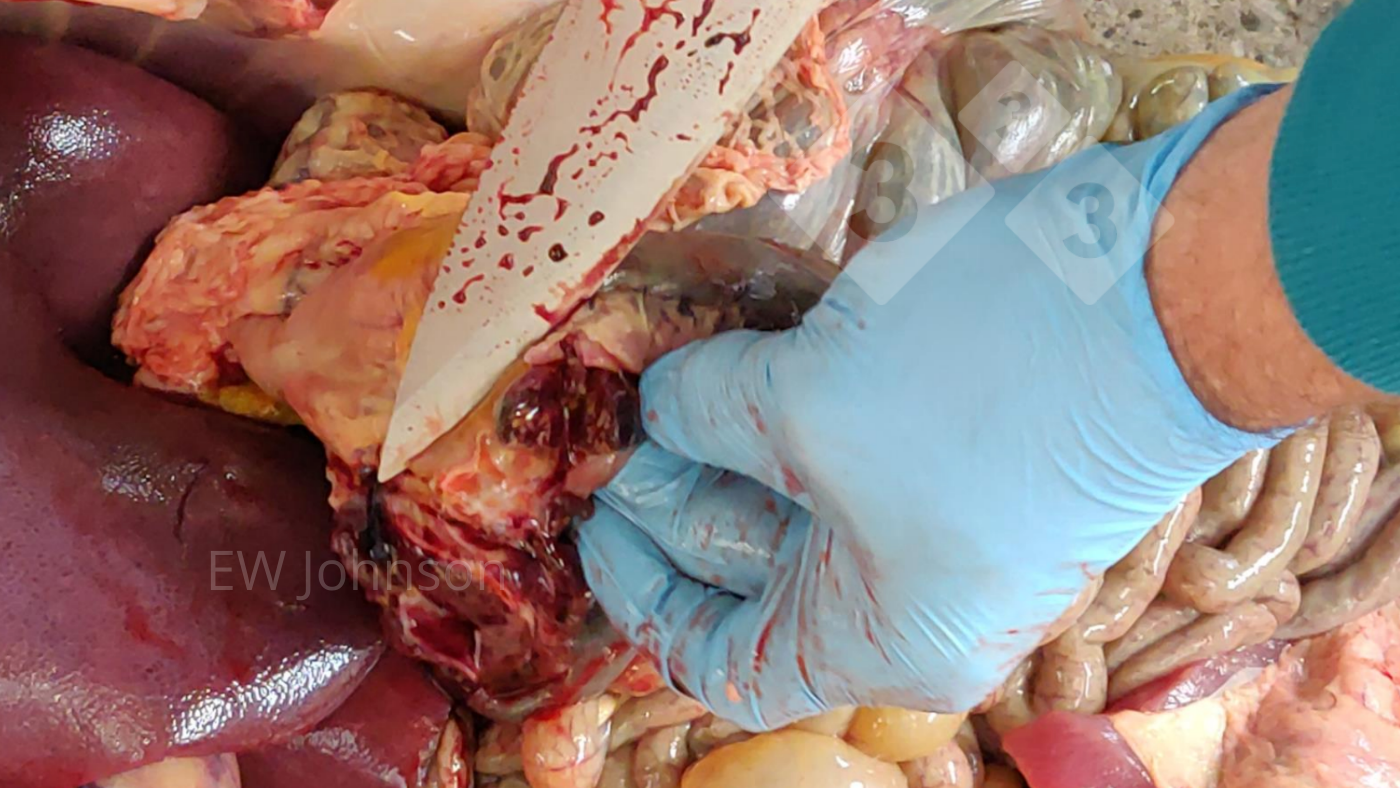
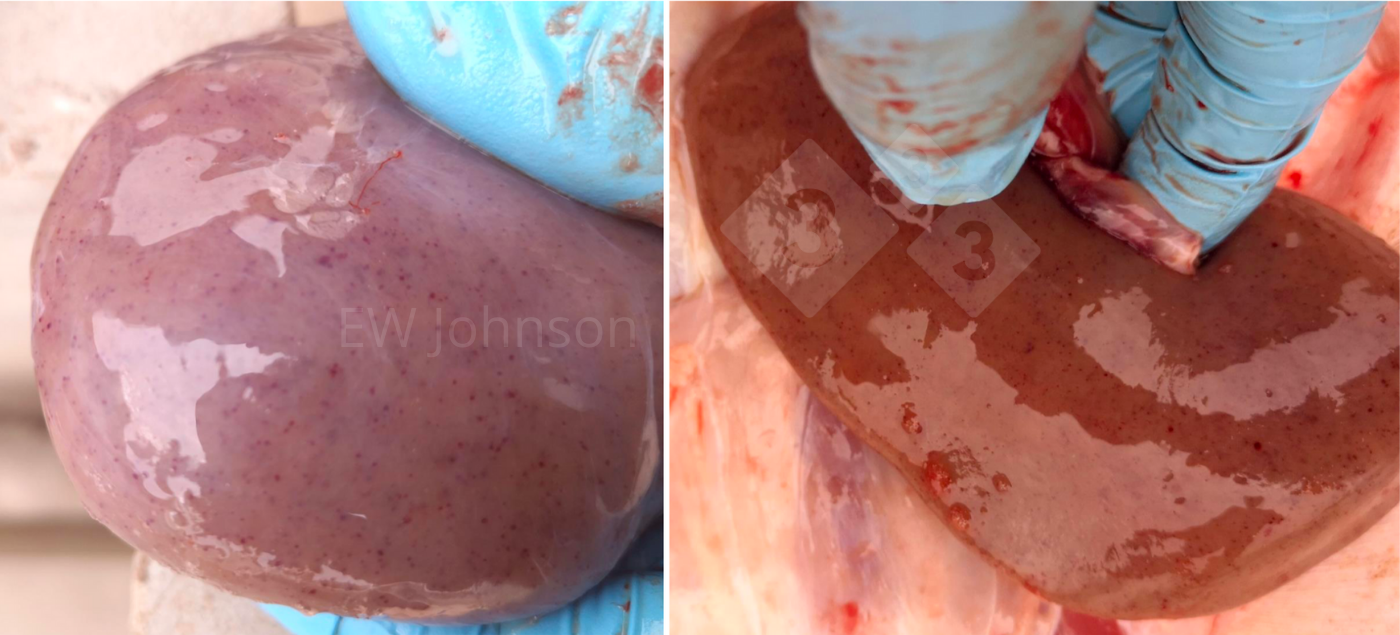 La severidad de las lesiones entre animales es variable y generalmente se sugiere que se necropsien varios cerdos.
La severidad de las lesiones entre animales es variable y generalmente se sugiere que se necropsien varios cerdos.
La necropsia debe realizarse con una preocupación profesional por la bioseguridad, aunque no presenta riesgos específicos en una granja ya infectada y proporciona información valiosa que no se puede obtener con acercamientos diagnósticos menos agresivos.
Técnicas laboratoriales
PCR: El diagnóstico de la PPA se suele verificar mediante una prueba de ácido nucleico positiva y descartando otras causas frecuentes que provocan lesiones similares. La más común es la PCR para el gen P72. El pulmón (muestra preferida en nuestro laboratorio), los riñones, el bazo, los linfonodos, el suero y la sangre, son todas muestras excelentes para PCR. Los hisopos y los fluidos orales son extremadamente populares, pero la cantidad de virus es varios logaritmos menor de que lo que se suele encontrar en sangre y tejidos, por lo que los falsos negativos son bastante comunes. Se utiliza qPCR de fluorescencia y PCR convencional. La PCR convencional ofrece una práctica vía para la secuenciación genética.
Cuando se usa deliberadamente una vacuna con el gen deleteado o se ha introducido accidentalmente la cepa del virus de la PPA con un gen deleteado, los tests de ácido nucleico pueden fallar en algunos animales porque la cantidad de virus que se produce es mucho menor en comparación con el virus de campo. Sin embargo, cuando se dispone de muestras apropiadas de tejido o sangre, se puede realizar un análisis de ácido nucleico para detectar los genes eliminados del virus de la vacuna. Si se obtiene un resultado positivo para el gen P72, se puede realizar una PCR para la vacuna con el gen eliminado en busca de la presencia de ADN de MGF 360-505 R y CD2v para determinar si el virus problema es el de campo o el de la vacuna con el gen deleteado.
Amplificación isotérmica mediada por bucle (LAMP): ofrece una alternativa de ácido nucleico rápida, barata, flexible y extremadamente sensible que requiere poco equipo especializado y parece adecuada para análisis masivos como la monitorización / detección en matadero.
Serología: puede usarse para determinar si los animales han estado expuestos al virus de la PPA cuando el tiempo transcurrido desde la infección hasta el test ha sido suficientemente largo como para que haya pasado el periodo de viremia y de presencia de virus en tejidos, o si no disponemos de buenas muestras de necropsia.
Hay varios kits ELISA disponibles para buscar la presencia de anticuerpos contra P72, P 30 y otros antígenos de la PPA. Estos tests a menudo se usan para identificar y, por lo general, eliminar grupos de cerdas que han sido vacunadas deliberadamente o que han sido expuestas accidentalmente al virus de la vacuna ilegal.
Hay un test rápido de captura de antígenos mediante ELISA, pero tiene muy poca sensibilidad, por lo que su uso se limita generalmente a casos en los que se desea un falso negativo rápido.
En el examen histopatológico se observa una vasculitis generalizada con infarto, hemorragia y trombosis en múltiples órganos, particularmente el pulmón, bazo, linfonodos, riñones, cerebro e intestino. Hay una destrucción linfoide masiva en los linfonodos y el bazo, y vacuolización de los macrófagos alveolares. Es frecuente la necrosis y la ulceración del epitelio del colon (foto 4).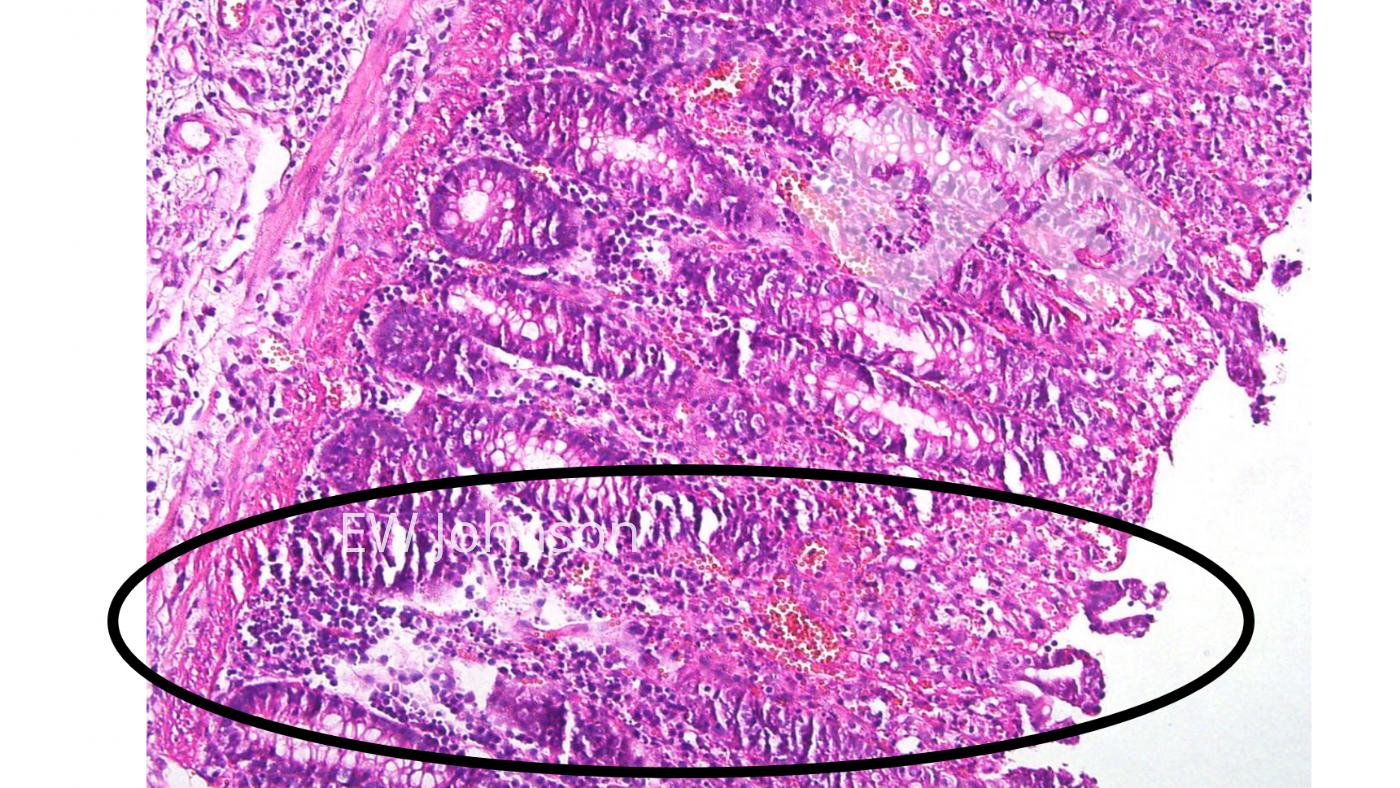
El uso de la histopatología para verificar las lesiones crónicas típicas de la vacuna con genes deleteados puede ser muy útil. Los cerdos que han recibido dichas vacunas de PPA suelen presentar lesiones vasculares fibrosantes y cicatrizantes crónicas activas que incluyen trombos e infartos en el intestino, el hígado, los tejidos linfoides, el corazón y los riñones. Los linfonodos pueden tener áreas hemorrágicas, con necrosis y destrucción linfocitaria y zonas con fibrosis y cicatrización. Los reproductores vacunados pueden presentar grandes zonas de necrosis pulmonar y fibrosis que a menudo se confunden con App crónica. Es posible que el virus de la vacuna no mate al cerdo, pero el cerdo a menudo no puede eliminar el virus de la vacuna.
Hay que recordar que la PCR es una gran herramienta, pero no es infalible y, en la situación actual de las granjas, no es 100% precisa. Esto no quiere decir que no sea una técnica en la que confiar, al contrario, pero aun así, los resultados de la PCR son los resultados de una prueba diagnóstica, no un diagnóstico. El encargado de hacer el diagnóstico debe investigar, debe utilizar todas las herramientas que estén a su disposición. Cuando se sospecha de PPA, deben tomarse medidas de bioseguridad, incluso más de las habituales. Pero hay varias enfermedades parecidas a PPA y además de que tengamos un test frente a PPA, se requiere un diagnóstico de la causa real del problema, lo que puede requerir más intervención y observación que extraer un linfonodo inguinal o exteriorizar el bazo a través de una pequeña incisión.
