Gestión del riesgo en seguridad alimentaria. La importancia del muestreo (I)
21-dic-2015 (hace 9 años 3 meses 13 días)
De acuerdo con los datos de enfermedades de transmisión alimentaria de los EE.UU., los microorganismos implicados no son estables, detectándose un incremento de los microorganismos que tienen un menor control y una reducción de aquellos que han estado sometidos a medidas de análisis y verificación más intensas. Este es el caso de Salmonella y Listeria monocytogenes. Estos microorganismos han reducido su prevalencia en la población americana en un 9% y un 3% respectivamente, según los datos del Centers for Disease Control and Prevention (CDC) del 2013 (Gráfica 1). Para Listeria, la tasa actual es de 0,26 por cada 100.000 habitantes. Considerando una población de unos 300 millones de habitantes, supone que 780 fueron afectados por este microorganismo. En nuestro país, el año 2012 tuvimos 129 casos, lo que supone una prevalencia de 0,32 casos por cada 100.000 habitantes.
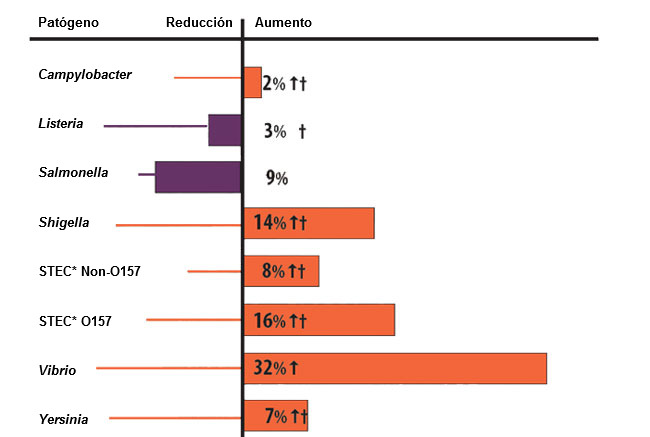
Gráfica 1. Cambios en las enfermedades de transmisión alimentaria en EE.UU. en 2013. Fuente: CDC (www.cdc.gov/foodnet)
Por tanto, el control es importante en la reducción de casos, detectando que la tasa de prevalencia en EE.UU. es inferior a la de nuestro país. Si a eso acompañamos que según las estadísticas oficiales, la mortalidad por este microorganismo se sitúa entorno al 30% de los afectados, podemos comprender que es uno de los microorganismos que provoca una mayor mortalidad en los países desarrollados, ligada a la transmisión alimentaria.
Importancia del APPCC
Para evitar este problema, el sistema que se ha mostrado más eficaz ha sido la aplicación del APPCC. En sus orígenes, cuando los niveles de contaminación son elevados, su implantación es relativamente sencilla, puesto que el análisis de un número relativamente bajo de muestras podría dar una idea de los niveles de contaminación reales de una planta. Sin embargo, esto no es así cuando después de la implantación de unas correctas medidas de higiene se consigue una reducción significativa de la presencia de este u otros patógenos. En estos casos, el enfoque tradicional del sistema no funciona.
Basta como ejemplo la idea de que la relación entre la presencia y la detección de un microorganismo en una muestra se mantiene siempre en una proporción constante o en una equivalencia 1:1. ¿Qué significa esto? Que si tenemos un lote de muestra, por ejemplo de 5, donde se detecta una presencia de un patógeno, al repetir el análisis de otras 5 muestras, se ha de encontrar obligatoriamente 1 muestra positiva. Esto no es así en todos los casos y depende de la frecuencia de presentación del microorganismo en el producto acabado. En este caso, los conceptos clásicos del sistema APPCC no funcionan y requieren entender cuál es la situación real y cómo afrontar los retos que tendremos delante, en seguridad alimentaria.
Curiosamente, este hecho está recogido en la legislación vigente. Así, el Reglamento 2073/2005 sobre criterios microbiológicos en productos alimenticios, ya recogía que para aceptar un lote para consumo humano, debía cumplir con los criterios señalados en la norma después de analizar 5 muestras, no debiendo detectar, por ejemplo, ninguna presencia. Este mismo hecho se ha ido recogiendo en el resto de normas relacionadas, como el Reglamento (UE) 365/2010 o el Real Decreto 135/2010, que modifican estos criterios. En ningún caso se recoge la posibilidad de conseguir la completa ausencia de patógenos en los alimentos, puesto que no es posible, técnicamente, al no existir el riesgo cero. Otra cuestión es poder llegar a alcanzar un riesgo técnico próximo a cero. Eso sólo se conseguirá cuando la presencia de un patógeno sea tan reducida que no sea posible su detección con las técnicas actuales.
Para ello, es importante entender la importancia del muestreo y su integración en el sistema APPCC, recogiendo los resultados históricos de los análisis de laboratorio, con la finalidad de crear alertas que nos permitan actuar cuando estemos ante una situación crítica y no cuando no sea necesario.
Muestreo
Si nos centramos en el caso de Listeria monocytogenes, la normativa europea es clara en la diferenciación entre aquellos casos en los que el patógeno no puede crecer en los alimentos, respecto a aquellos en los que el patógeno sí puede crecer. En el primer supuesto se pide la ausencia del patógeno, en 5 muestras, en el momento de elaborar un alimento. Sin embargo, se acepta la presencia de menos de 100 ufc/g al terminar la vida comercial. Si nos detenemos a pensar este criterio, debemos entender cómo es esto posible. Según los criterios clásicos, si hay ausencia, no puede estar presente el microorganismo, por aquella idea comentada de la relación 1:1 entre los diferentes lotes de muestra. Si eso fuera así ¿cómo puede haber presencia de un lote donde hemos detectado ausencia? La razón, a mi entender, es clara, porque podemos tener ausencia en 5 muestras pero presencia en 1 de 10 ó 1 de 100 ó 1 de 1.000. Sólo con que en un lote de 20.000Kg de producto hubiese una sola Listeria, esta se podría multiplicar hasta miles de millones de individuos idénticos si se producen las condiciones adecuadas, como puede ser la rotura de la cadena de frío. Por tanto, es posible, las autoridades sanitarias europeas lo identificaron, debiendo mantener todas aquellas condiciones que limitan el crecimiento del patógeno. Por tanto, consideraron un nivel de riesgo aceptable, que en 5 muestras de un lote, ninguna tuviera presencia, pero no hay opinión sobre si la presencia fuera de 1 en 100 muestras. En este caso el lote sería aceptable, como espero poder explicar más adelante, en la segunda parte del artículo.
Si nos fijamos en lo que ocurre en aquellos productos en los que Listeria monocytogenes no puede crecer, el límite legal se ajusta a 100 ufc/g en 5 muestras desde el principio al final de la vida comercial. En consecuencia, el riesgo no está ligado sólo a la presencia, sino a un número concreto de microorganismos.
