¿Podemos controlar la circovirosis porcina? ¿Erradicación?
13-sep-2007 (hace 17 años 6 meses 21 días)
Factores de riego
El control de enfermedades consideradas multifactoriales, como la circovirosis porcina, debe enfocarse de forma multifactorial. Es decir, es difícil pensar a priori que soluciones puntuales y únicas sean capaces de solucionar la problemática clínica.
Tal como se ha citado en el apartado de patogenia, existen una serie de factores y/o acciones que algunos estudios han relacionado con desencadenamiento, modulación y/o protección frente a la circovirosis porcina.
Desde el punto de vista epidemiológico solamente alguno de esos puntos han sido demostrados, y no siempre en todos los estudios (existencia de datos contradictorios), como factores potenciales de riesgo real. Entre ellos cabe destacar:
 |
 |
|
 |
El resto de factores o efectos corresponderían a situaciones que modifican, para bien o para mal, desde el punto de vista natural o experimental, la situación final de enfermedad en granja. También se han descrito datos contradictorios a este nivel, pero dado que son factores potencialmente modificables por el veterinario y granjero/a, se citan en este apartado y son discutidos en los apartados siguientes. Entre ellos se destaca:
|
- Medidas de manejo - Nutrición - Vacunación frente a PCV2 - “Sueroterapia” - Efecto de la genética del cerdo - ¿Cepa de PCV2? - ¿Efecto granja? |
 |
De hecho, la mayoría de los puntos aquí citados tienen una implicación directa o indirecta con el sistema inmune de los cerdos. Por tanto, es de esperar que en los próximos años se dedique un marcado interés científico al estudio de la respuesta inmune del cerdo frente a la infección por PCV2.
A efectos prácticos, se recomienda que el establecimiento de pautas de control y prevención frente a la circovirosis porcina se base en la modulación de aquellos factores que se sabe están involucrados en la ocurrencia de la enfermedad.
Efecto del manejo



|
|
 |
|
|
El Dr. Madec fue el primer ciéntífico que contribuyó a desarrollar un plan de manejo para el control de la circovirosis porcina.
| El plan de 20 puntos de Madec |
| Área de parideras: |
| 1. Realizar un manejo “todo dentro-todo fuera”, y vaciar, limpiar y desinfectar las fosas de purines entre lotes. |
| 2. Lavar las cerdas y desparasitarlas antes de parir. |
| 3. Utilizar adopciones solamente en caso necesario, y únicamente en las primeras 24 horas post-nacimiento. |
| Área de transición: |
| 4. Corralinas pequeñas y con particiones sólidas. |
| 5. Vaciar, limpiar y desinfectar las fosas de purines entre lotes, y realizar un estricto manejo “todo dentro-todo fuera”. |
| 6. Disminuir la densidad de animales por corralina (=3 lechones/m2). |
| 7. Incrementar el espacio de comedero por cerdo (>7cm/lechón) |
| 8. Mejorar la calidad del aire (NH3<10 ppm; CO2<0,1%; humedad relativa<85%, etc.) |
| 9. Mejorar el control de temperatura. |
| 10. No mezclar lotes. |
| Área de engorde y finalización: |
| 11. Corralinas pequeñas y con particiones sólidas. |
| 12. Vaciar, limpiar y desinfectar las fosas de purines entre lotes, y realizar un estricto manejo “todo dentro-todo fuera”. |
| 13. No mezclar con cerdos que procedan de la transición. |
| 14. No remezclar entre cerdos de distintas corralinas de finalización. |
| 15. Disminuir la densidad de animales por corralina (>0,75 m2/cerdo). |
| 16. Mejorar la calidad del aire y la temperatura. |
| Puntos adicionales: |
| 17. Programa vacunal apropiado. |
| 18. Adecuado flujo entre edificios (de animales, de aire, etc.). |
| 19. Higiene estricta (en el corte de colas y colmillos, durante las inyecciones, etc.). |
| 20. Rápida separación de los cerdos enfermos a las dependencias hospitalarias que se tengan, o bien eutanasia de los mismos. |

Todas las medidas propuestas se encuentran dirigidas a reducir la “presión de infección” en relación a PCV2 y a cualquier otro agente patógeno, así como mejorar la higiene y reducir el estrés de los animales en las distintas fases de producción.
Infecciones concomitantes con PCV2
 |
|
Virus del PRRS, parvovirus porcino y Mycoplasma hyopneumoniae se consideran agentes infecciosos que potencialmente pueden desencadenar la circovirosis porcina en cerdos infectados con PCV2.
|
Tanto los estudios epidemiológicos como experimentales indican que la co-infección de PCV2 con PPV, PRRSV o Mycoplasma hyopneumoniae corresponderían a factores de riesgo para el desarrollo de la circovirosis porcina.
El mecanismo por el cual se da esta potenciación es desconocido pero se ha hipotetizado que tanto PPV como el PRRSV podrían "activar" macrófagos, facilitando así la replicación de PCV2.

Por tanto, si ciertas co-infecciones víricas en cerdos ya infectados con PCV2 pueden desencadenar la circovirosis porcina, sería de esperar que el control de estas infecciones concomitantes suponga, indirectamente, el control o minimización de la enfermedad (en aquellas granjas donde, lógicamente, se confirme la co-infección correspondiente).
Estimulación del sistema inmunitario: ¿efecto de las vacunaciones?
Aunque la “hipótesis de la inmuno-estimulación” para el desencadenamiento de la circovirosis porcina ha sido demostrada en algunos estudios experimentales y de campo, otros estudios no la han confirmado.
Por tanto, podría ser que, en ciertas circunstancias, la activación del sistema inmune a través de vacunas, productos estimuladores del sistema inmune u otras situaciones, podría suponer una potenciación de la circovirosis porcina. El problema es que estas “circunstancias” no han sido aún esclarecidas.
 |
 |
|
Se recomienda a veterinarios y granjeros que consideren la determinación aproximada del momento de infección por PCV2 para que así, en aquellos casos donde la circovirosis porcina sea significativa, se pueda reevaluar el momento óptimo de aplicación de productos vacunales.
|
Por otro lado, definitivamente, también es de lógica el hecho de no vacunar (equivalente a “inmunoestimular”) animales que se encuentren enfermos, sea por circovirosis porcina o por cualquier otra enfermedad.
En ningún caso se recomienda que, ante una situación de circovirosis porcina, se retire la aplicación de productos vacunales que se usan en la granja y cuya retirada pueda suponer un problema aún más grave que el que implica la circovirosis porcina.
Efecto de la nutrición

Se ha propuesto que el uso de ciertos nutrientes así como de aditivos con propiedades antioxidantes pueda ayudar a paliar una situación clínica de circovirosis porcina.
Un estudio reciente ha demostrado que el uso de ácido linoleico conjugado en la dieta de animales infectados con PCV2 disminuye las lesiones microscópicas observadas en la circovirosis porcina, así como mejora algunos parámetros inmunológicos.
 Actualmente no existe prácticamente base científica en relación a qué elementos nutricionales presentan un efecto protector/desencadenante de la circovirosis porcina.
Actualmente no existe prácticamente base científica en relación a qué elementos nutricionales presentan un efecto protector/desencadenante de la circovirosis porcina.
Sueroterapia
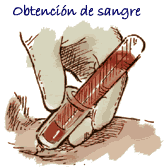
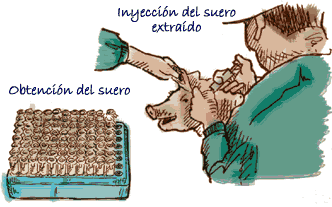
Hace unos pocos años se demostró que la inyección subcutánea de suero de cerdos de matadero en lechones de lactación o transición permitía reducir substancialmente la mortalidad asociada a circovirosis porcina.
Para la aplicación de esta metodología es muy importante tomar precauciones estrictas en relación a la toma de sangre y para su desuerado, así como evitar el riesgo de contaminaciones del suero obtenido (tratamiento antibiótico), etc.
 |
 |
El éxito de la “sueroterapia” ha sido muy variable; en algunas granjas ha permitido reducir significativamente los niveles de mortalidad mientras que en otras no se ha observado ningún efecto positivo.
El mecanismo de acción potencial de esta "sueroterapia" es desconocido. Se debe valorar muy cuidadosamente el riesgo de introducción de otros patógenos, potencialmente presentes en cerdos de engorde, a los cerdos que reciben el suero.
Estado de infección de la cerda frente a PCV2 al parto
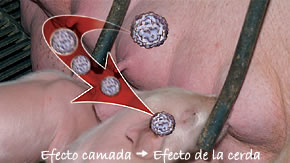
Se ha observado que los cerdos que mueren de circovirosis porcina corresponden solamente a ciertas camadas, hecho que sugiere la posible existencia de un “efecto camada” en relación a esta enfermedad.
Es más, este posible efecto no tiene aparentemente nada que ver con el número de parto de la cerda.
Recientemente, se ha demostrado que el estado de infección de la cerda poco después del parto en relación a PCV2 (medido como una PCR positiva en suero frente al virus) se asociaba significativamente con una mayor mortalidad entre los lechones correspondientes a la cerda infectada.
 |
En base a estos resultados, cualquier factor que permita disminuir la viremia alrededor del parto podría tener efectos protectores frente al desarrollo de la circovirosis porcina.
→ ¿Efecto potencial de una vacuna frente a PCV2 utilizada en cerdas?
Título de anticuerpos de la cerda frente a PCV2 al parto
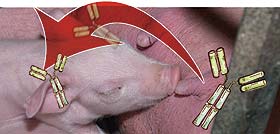
En un par de estudios se ha demostrado también que una mayor proporción de cerdos nacidos de madres con títulos serológicos bajos frente a PCV2 morían de circovirosis porcina.
| La inmunidad maternal se considera protectora en relación al desarrollo de la circovirosis porcina |
En base a estos resultados, cualquier factor que permita incrementar los títulos de anticuerpos frente a PCV2 en cerdas alrededor del parto podría tener efectos protectores frente al desarrollo de la circovirosis porcina.
→ ¿Efecto potencial de una vacuna frente a PCV2 utilizada en cerdas?
No obstante, también se han descrito situaciones donde el efecto de la inmunidad maternal aparentemente no se relacionaba con protección frente a la circovirosis porcina.
 |
Vacunación frente a PCV2
 Se han desarrollado algunas estrategias vacunales frente a PCV2 desde el punto de vista experimental, que incluyen:
Se han desarrollado algunas estrategias vacunales frente a PCV2 desde el punto de vista experimental, que incluyen:
|
- Vacunas inactivadas - Vacunas recombinantes - Vacunas DNA - Vacunas basadas en clones infecciosos |
Todas ellas han mostrado cierto efecto protector, sea a través de la disminución de la intensidad de las lesiones linfoides características de la circovirosis porcina o bien por la disminución del número de animales que sufren enfermedad, una vez desafiados con cepas de campo de PCV2.

Actualmente existe una vacuna inactivada y adyuvantada frente a PCV2* (CIRCOVAC®, Laboratorios Merial) que se comercializa bajo licencia especial temporal en algunos países de la Unión Europea. Ello está permitiendo analizar la eficacia real de este producto vacunal en condiciones de campo.
*Ver artículo de C. Charreyre, página 160. CIRCOVAC®, es una marca registrada de Merial, Lyon, Francia.
Efecto de la genética
 |
|
German Landrace
|
 |
|
Duroc
|
 |
|
Berkshire
|
 |
|
Piétrain
|
Algunas observaciones de granjeros y veterinarios han sugerido que ciertas líneas genéticas, especialmente en relación al verraco, se asocian a mayores o menores incidencias de circovirosis porcina en transición y engorde.
No obstante, a día de hoy no existe prácticamente información científica contrastada en relación a este tema, aunque es bastante improbable que una raza específica pueda ser identificada como intrínsecamente resistente a la circovirosis porcina.
Solamente existen unos pocos estudios contrastados en relación al posible efecto de la genética:
• En España (estudio de campo): confirmación de la existencia de un efecto significativo de la línea genética paterna sobre la mortalidad post-destete y la circovirosis porcina; este efecto se asoció aparentemente a la línea genética determinada utilizada en las granjas de estudio mucho más que a una raza en concreto.
• En Francia (estudio de campo): no se confirmó que la raza Pietrain produzca un efecto protector en relación al desarrollo de la circovirosis porcina.
• En Estados Unidos (estudio experimental): cerdos de raza Landrace mostraron mayor intensidad lesional en órganos linfoides que cerdos de razas Duroc o Large White, frente al desafío con PCV2.
Parece relativamente claro que existe un efecto asociado a la genética de los cerdos en relación al desarrollo de la circovirosis porcina. No obstante, este efecto no ha sido aún esclarecido ni precisado.
Si ello es posible, en una granja con graves problemas de circovirosis porcina, se sugeriría el cambio de la línea genética paterna como posible efecto de paliación de la enfermedad.
¿Efecto de la cepa de PCV2?
Las distintas cepas de PCV2 presentan en general una homología nucleotídica superior al 94%, lo que indica una similitud muy grande entre los distintos aislados a nivel mundial.
 Dendrograma circular correspondiente a 131 cepas de PCV2 totalmente secuenciadas y disponibles en el GenBank. Las distintas cepas de PCV2 muestran una homología nucleotídica que varia entre el 94,2 y el 99,8%. Esta identidad, en cambio, es del 75,0 y el 76,3% cuando se comparan con PCV1. |
Inicialmente se concluyó que esta similitud probablemente no contribuiría de forma significativa a las diferencias en expresión de la enfermedad entre las granjas o incluso a las diferencias entre granjas infectadas con PCV2 con y sin circovirosis porcina.
Un estudio demostró también que una cepa de PCV2 procedente de un cerdo sano de un país que al momento de aislamiento del virus no había descrito casos de circovirosis porcina (Suecia) es capaz de generar enfermedad en condiciones experimentales. Por tanto, se concluyó que, probablemente, cualquier cepa de PCV2, en las condiciones adecuadas, es capaz potencialmente de producir circovirosis porcina.
Actualmente se está estudiando la posible diferencia de patogenicidad entre cepas de PCV2:
|
|
 |
 |
 |
¿Efecto de la granja?
 Observaciones e impresiones de los veterinarios de campo han mostrado que la expresión de la circovirosis porcina puede variar según granja.
Observaciones e impresiones de los veterinarios de campo han mostrado que la expresión de la circovirosis porcina puede variar según granja.
Estos datos han sido corroborados epidemiológicamente. Los estudios estadísticos de modelización de enfermedades indican que al igual que se ha descrito un efecto de la cerda, un efecto de la genética, etc., existe un efecto granja en relación a la ocurrencia de circovirosis porcina.
Actualmente se desconoce los elementos intrínsecos que podrían definir este efecto granja; a pesar de que el manejo podría ser uno de ellos, también podría haber muchos otros aún no determinados (bioseguridad, instalaciones, densidad de animales, etc.).
Erradicación de la circovirosis porcina: ¿tiene sentido?
Erradicación:
Supresión total de la transmisión de una enfermedad entre los animales de una población, a través de la eliminación (exterminación) del agente patógeno.
Si atendemos a lo descrito para otras enfermedades de los cerdos, algunas de las estrategias de erradicación incluirían:
|
1. Despoblación total y repoblación. 2. Test y eliminación de los animales positivos. 3. Cerrado de la granja con objeto de estabilizar la infección. 4. Producción de cerdos negativos a partir de cerdas positivas. |

Teniendo en cuenta que PCV2 es un virus…
→ Ubicuo (es prácticamente imposible encontrar granjas seronegativas).
→ Altamente contagioso (una vez se infectan los primeros cerdos, se infectarán en un corto período de tiempo todos los animales del grupo).
→ Altamente infeccioso (dosis bajas del virus permiten la infección del animal).
→ Muy resistente (a la mayoría de desinfectantes y en el medio ambiente).
…parece relativamente claro que erradicar la infección por PCV2 puede ser una tarea prácticamente imposible y, a priori, quizás muy poco útil, dado que el riesgo de reinfección es aparentemente muy elevado. Por tanto, definitivamente es muy difícil (o imposible) justificar económicamente una acción orientada a la erradicación de la infección por PCV2.
 |
 |
|
Paridera que podría ser resultante de un proceso de despoblación total.
|
No obstante, ¿es factible erradicar la infección por PCV2?
1. Despoblación total y repoblación
Aparentemente sería la mejor opción, pero ¿de donde se saca una fuente de animales negativos frente a PCV2?
2. Test y eliminación de los animales positivos
No parece una opción demasiado factible, dado que al ser un virus ubicuo va a ser muy difícil que no se den reinfecciones constantes dentro de la misma granja. En último caso, y en la mayoría de las granjas convencionales, el número de cerdas y verracos positivos son generalmente más del 80%, por lo que esta opción no es factible. Se considera que la opción de “test y eliminación” es económicamente viable si el porcentaje de animales positivos es menor al 10%. Y, al igual que en el caso anterior, tampoco se garantiza la disponibilidad de una fuente de animales negativos frente a PCV2.
 3. Cerrado de la granja con objeto de estabilizar la infección.
3. Cerrado de la granja con objeto de estabilizar la infección.
Actualmente ya se sabe que ello no provoca el cese de la transmisión de la infección por PCV2. Esta situación, dado que permite estabilizar la granja frente a otras infecciones como la causada por el PRRSV, puede, secundariamente, suponer una disminución del impacto clínico de la circovirosis porcina pero la infección con PCV2 se da igualmente. Al igual que en los casos anteriores, tampoco se garantiza la disponibilidad de animales negativos frente a PCV2.
4. Producción de cerdos negativos a partir de cerdas positivas.
Esta sería probablemente la opción más realista, y a día de hoy se sabe que sí es posible. No obstante, ello ha de implicar la no existencia de circulación de PCV2 entre las cerdas ni entre los lechones de paridera. En este contexto, la segregación de los animales al destete permite potencialmente criar animales hasta matadero sin que se produzca la infección por PCV2. Otra cuestión sería ¿con qué frecuencia tiene éxito esta práctica? Actualmente ello es desconocido.
 Finalmente, en caso de lograr erradicación de la infección por PCV2 en una granja, ¿Cómo se evita la reinfección por PCV2 teniendo en cuenta que es un virus que se transmite, aparentemente, muy fácilmente?
Finalmente, en caso de lograr erradicación de la infección por PCV2 en una granja, ¿Cómo se evita la reinfección por PCV2 teniendo en cuenta que es un virus que se transmite, aparentemente, muy fácilmente?
Definitivamente, y en la actualidad, hablar de erradicación de la infección por PCV2 parece no tener demasiado sentido, ni económico, ni práctico.
