Visita a la granja: ¿Cuándo sospechar?
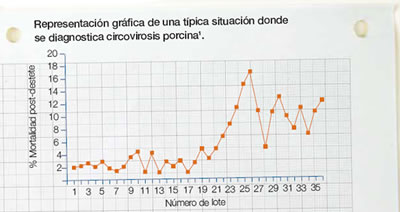
La sintomatología clínica más característica de una granja con circovirosis porcina corresponde a un incremento del porcentaje de cerdos de transición y/o engorde con retraso en el crecimiento (y por tanto un aumento del número de “colas” o “saldos”) y un incremento de la mortalidad, generalmente asociada a este desmedro.

 |
|
1Esta granja, a partir del lote número 22, experimentó un incremento marcado de la mortalidad post-destete, asociada básicamente a cerdos con desmedro.
|
  |
|
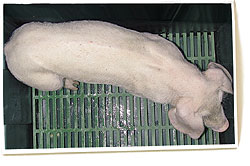
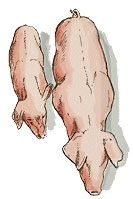
Cerdos de 2 (izquierda) y 3 meses (derecha) con circovirosis porcina. Nótese la espina dorsal marcada, indicativa de retraso en el crecimiento.
|
 |
|
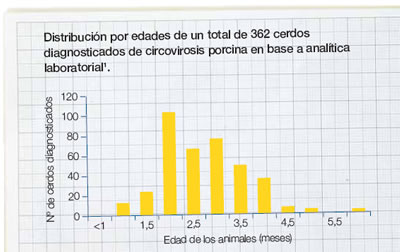
1Se observa que el 90% de los casos se reparten entre 2 y 3,5 meses de edad.
(Fuente: Servicio de Diagnóstico Patológico de la Facultad de Veterinaria de Barcelona) |
Otros síntomas clínicos que aparecen en la circovirosis porcina, aunque con una frecuencia variable, serían:
| Síntoma clínico | Frecuencia relativa en los cerdos con circovirosis porcina |
| Alteraciones respiratorias (disnea) | 70-80 % |
| Palidez corporal (anemia) | 60-70 % |
| Linfadenopatía inguinal (incremento de tamaño de los linfonodos inguinales superficiales) | 40-60 % |
| Alteraciones digestivas (diarrea) | 10-30 % |
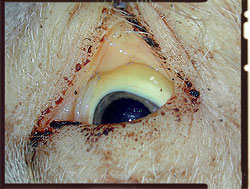
| Coloración amarillenta de la canal y especialmente de la grasa (ictericia) | 1-5 % |
 |
|
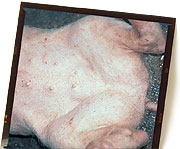
Cerdo de 3 meses con circovirosis porcina. Nótese la espina dorsal marcada, indicativa de retraso en el crecimiento, y la palidez corporal (anemia).
|
 |
|
|
 |
|
Concomitantemente, los cerdos de una granja afectada con circovirosis porcina pueden presentar otras enfermedades que cursen, a su vez, con otros síntomas clínicos. Por tanto, el cuadro clínico final resultante será una mezcla de todo aquello que, en un momento dado, sufran los animales de la granja correspondiente.
|
 |
 |
Desde el punto de vista epidemiológico existe una serie de datos que permitirían, conjuntamente con la sintomatología clínica, sospechar de forma relativamente clara de un caso de circovirosis porcina.
|

|
| Aspectos epidemiológicos a considerar como importantes en la circovirosis porcina | |
| Afectación | Individual: es habitual ver unos pocos animales de cada corralina con el cuadro clínico |
| Edad de afectación | Usualmente entre 6 y 14 semanas de vida (casos extremos hasta las 18-20 semanas de vida) |
| Cerda (“efecto de la cerda” o “efecto camada”) | Lechones procedentes de cerdas infectadas con PCV2 alrededor del parto o con un bajo título de anticuerpos frente a este virus son más susceptibles a sufrir la enfermedad |
| Sexo | Mayor mortalidad en machos que en hembras |
| Morbilidad | Variable, aunque generalmente entre 4-30% (casos extremos hasta el 60-70%) |
| Tasa de recuperación | Aproximadamente un 30-70% de los animales sobreviven; quedando el resto como “saldos” o “colas” |
| Genética | Aparentemente existen líneas genéticas con mayor susceptibilidad que otras; muy poco estudiado |
| Respuesta al tratamiento antibiótico | Prácticamente ausencia de respuesta al tratamiento; efecto potencialmente visible en aquellas granjas donde exista una elevada cantidad de procesos concomitantes de origen bacteriano |
| Duración del proceso clínico en un lote de animales | Generalmente 1 a 2 meses |
| Duración del proceso clínico en una granja | Muy variable, desde afectación solamente de 1 o 2 lotes hasta valores significativamente incrementados de mortalidad y desmedro durante 2-3 años |
Necropsia de animales afectados
A pesar de que la sintomatología de la circovirosis porcina así como también las lesiones macroscópicas pueden variar significativamente de una granja a otra, aún teniendo la misma enfermedad, existen unos hallazgos de necropsia que tienden a facilitar un posible diagnóstico de la enfermedad.
De hecho, los hallazgos macroscópicos más representativos de la circovirosis porcina, además de la emaciación, son:
|
1. Linfadenopatía generalizada (incremento de tamaño generalizado de los nódulos linfáticos).
2. La ausencia de colapso pulmonar, con o sin patrón lobulillar evidente. 3. Existen otras lesiones macroscópicas que, aunque menos frecuentes, también se pueden observar en la circovirosis porcina. |
 |
 |
|
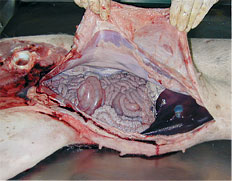
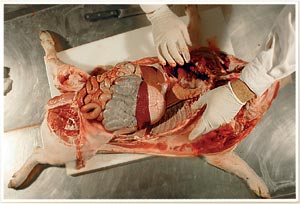
Apertura de la cavidad abdominal durante una necropsia
|
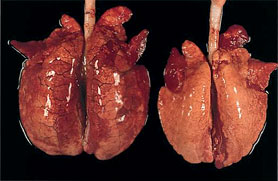
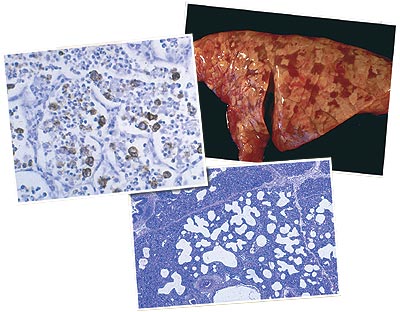
Pulmones correspondientes a dos animales con circovirosis porcina. El pulmón de la izquierda presenta marcada ausencia de colapso pulmonar con edema intersticial; ambas lesiones son altamente sugerentes de neumonía intersticial. El pulmón de la derecha presenta consolidación pulmonar craneo-ventral.
|
Frecuencia de las lesiones macroscópicas en 396 cerdos afectados de circovirosis porcina (Segalés et al., 2004)
| Lesión | Frecuencia | Porcentaje |
| Espina dorsal marcada (emaciación) | 318 | 80,3 |
| Ausencia de colapso pulmonar | 255 | 64,4 |
| Consolidación pulmonar craneo-ventral | 235 | 59,3 |
| Linfadenopatía regional o generalizada | 209 | 52,8 |
| Úlcera gástrica en la pars esofágica | 113 | 28,5 |
| Serositis (mono o poliserositis) | 99 | 25,0 |
| Atrofia serosa de la grasa | 90 | 22,7 |
| Riñones con focos blanquecinos multifocales | 73 | 18,4 |
| Heces rectales pastosas (colitis catarral) | 44 | 11,1 |
| Atrofia hepática | 13 | 3,3 |
| Colitis fibrino-necrotizante | 13 | 3,3 |
| Coloración amarillenta de la grasa (ictericia) | 12 | 3,0 |
| Necrosis de los nódulos linfáticos | 9 | 2,3 |
| Neumonía necrotizante | 8 | 2,0 |
| Hepatomegalia | 2 | 0,5 |
¿Cómo interpretar las lesiones macroscópicas observadas?
Espina dorsal marcada (emaciación):
Efecto habitual en la infección por PCV2 en animales que desarrollan clínicamente la circovirosis porcina.
Ausencia de colapso pulmonar:
Muy probable neumonía intersticial. Efecto habitual por la infección por PCV2, aunque también puede ser causado por distintos agentes víricos, entre otros el virus del síndrome respiratorio y reproductivo porcino (PRRSV), o incluso ser el efecto sumatorio de distintos agentes víricos.
Consolidación pulmonar craneo-ventral:
Bronconeumonía catarral-purulenta, o lo que es lo mismo, infección bacteriana pulmonar. Supone una co-infección bacteriana en un caso de circovirosis porcina. NO es una lesión causada por PCV2, aunque pueda ser facilitada por un estado de inmunosupresión, hecho asumido en la circovirosis porcina.
 |
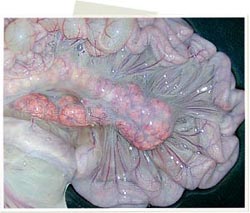
Linfadenopatía regional o generalizada:
Efecto característico de la infección por PCV2 en animales que desarrollan clínicamente la circovirosis porcina; se debe a un cambio en las subpoblaciones de órganos linfoides, siendo la inflamación granulomatosa la responsable del incremento de tamaño final de los nódulos linfáticos.
 |
|
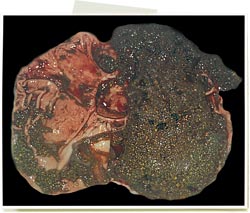
Úlcera gástrica en la pars esofágica:
Patología de origen multifactorial. Se presume que esta lesión presenta una elevada frecuencia en la circovirosis porcina dado que, al producir un estado de emaciación y, por tanto, de relativo ayuno prolongado, se genera una úlcera de tipo péptico. NO es una lesión causada por PCV2.
 |
|
Serositis (mono o poliserositis):
Infección bacteriana sistémica con afectación de una o varias serosas. Puede tratarse de lesiones de tipo fibrinoso (agudas), en las cuales tiene sentido intentar aislar el agente causante de las mismas, o de tipo fibroso (crónicas), donde el agente es difícilmente o muy difícilmente recuperable. La causa más frecuente de las mismas suelen ser bacterias como Haemophilus parasuis o Streptococcus suis. NO es una lesión causada por PCV2.
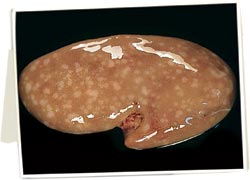
Riñones con focos blanquecinos multifocales:
Muy probablemente nefritis intersticial. Es una lesión habitual que se asocia a la infección por PCV2, pero que puede deberse a otras causas, muchas de ellas mal determinadas.
 |
|
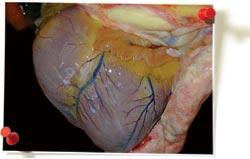
Atrofia serosa de la grasa:
Gelatinización de la grasa debido a la movilización de las grasas de reserva en un animal que va perdiendo peso y muestra emaciación. Es un efecto habitual de animales con circovirosis porcina que no mueren en fase aguda-subaguda y tienden a cronificarse.
 |
|
Heces rectales pastosas (colitis catarral):
Diarrea de origen potencialmente muy variable. Solamente se puede establecer un diagnóstico preciso en base a estudios laboratoriales, dado que la lista de los agentes infecciosos que potencialmente pueden dar este cuadro es relativamente amplia. Tampoco se debe olvidar que alteraciones nutricionales también generan un cuadro diarreico similar. PCV2 puede ser causa de diarrea en aquellos casos donde se observe una entero-colitis granulomatosa, hecho que habitualmente es raro.
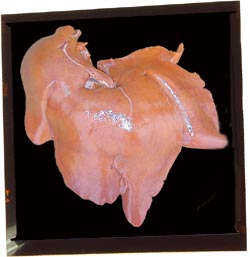
Atrofia hepática / hepatomegalia:
Efecto ocasional o muy ocasional en la infección por PCV2 en animales que desarrollan clínicamente la circovirosis porcina y que muestran ictericia, y por tanto, coloración amarillenta de la grasa. Sistemáticamente corresponde a una inflamación (hepatitis) grave del hígado.
 |
|
Colitis fibrino-necrotizante:
Infección bacteriana intestinal, siendo las causas más probables las infecciónes por Salmonella spp. y Brachyspira hyodysenteriae. NO es una lesión causada por PCV2.
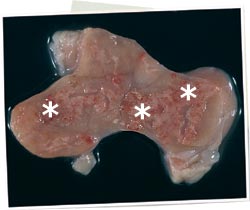
Necrosis de los nódulos linfáticos:
Efecto ocasional o muy ocasional en la infección por PCV2 en animales que desarrollan clínicamente la circovirosis porcina.
 |
|
Neumonía necrotizante:
Infección bacteriana respiratoria, siendo las causas más probables las infecciones por Actinobacillus pleuropneumoniae y Pasteurella multocida.
NO es una lesión causada por PCV2.
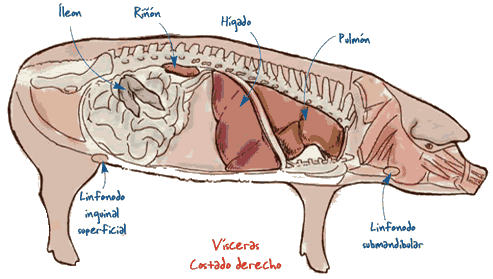
| Órganos donde se pueden potencialmente encontrar lesiones asociadas a la circoviroisis porcina |
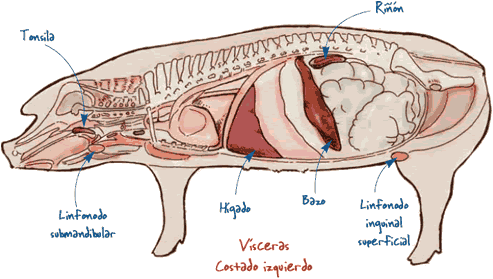 |
| Órganos donde se pueden potencialmente encontrar lesiones asociadas a la circoviroisis porcina |
 |
Diagnóstico diferencial
El diagnóstico diferencial de la circovirosis porcina puede ser muy amplio dependiendo del signo clínico dominante en cada granja en concreto, aunque en todos los casos debe incluirse un diagnóstico diferencial de las enfermedades que cursan con desmedro.
La primera y más importante entidad clínica a incluir en la lista de diagnóstico diferencial es la forma respiratoria del síndrome respiratorio y reproductivo porcino (PRRS). No obstante, la amplia distribución del PRRS en muchos países donde también existe circovirosis porcina hace muy difícil diferenciar entre una y otra enfermedad, a no ser que se utilicen a la vez las baterías de tests diagnósticos laboratoriales para las dos enfermedades.
 |
|
| Principales enfermedades del ganado porcino que cursan con desmedro en las fases de transición y/o engorde |
| Síndrome respiratorio y reproductivo porcino (forma respiratoria) |
| Enfermedad respiratoria genérica |
| Enfermedad de Glässer |
| Colibacilosis post-destete |
| Adenomatosis intestinal porcina (infección por Lawsonia intracellularis) |
| Intoxicación por carbadox / olaquindox |
| Úlcera gástrica de la pars esofágica |
| Disentería porcina, infección por Brachyspira hyodysenteriae |
| Espiroquetosis intestinal porcina, infección por Brachyspira pilosicoli |
| Eperitrozoonosis |
Toma de muestras y solicitud
La toma de muestras para confirmar la sospecha de circovirosis porcina dependerá directamente de nuestro objetivo básico:
 1 Confirmar o descartar la existencia de circovirosis porcina solamente (DIAGNÓSTICO DE CIRCOVIROSIS PORCINA).
1 Confirmar o descartar la existencia de circovirosis porcina solamente (DIAGNÓSTICO DE CIRCOVIROSIS PORCINA).
2 Confirmar o descartar la existencia de circovirosis porcina en el marco de un cuadro clínico de granja donde, con probabilidad, existen otros procesos patológicos (DIAGNÓSTICO GLOBAL).
Para el diagnóstico de la circovirosis porcina se puede plantear un estudio histopatológico relativamente amplio (tabla de toma de muestras más apropiadas) o bien un estudio “minimalista” (incluyendo solamente un par de órganos linfoides, preferiblemente un par de nódulos linfáticos o nódulo linfático y tonsila).
Muestras más apropiadas para la realización del diagnóstico histopatológico de la circovirosis porcina
| Tejidos | Características de la muestra* |
| Nódulos linfáticos | Enteros (linfonodos inguinal superficial, mesentérico, submandibular y mediastínico). |
| Tonsila | Entera. |
| Íleon | Una sección de unos 10 cm de longitud y abierta longitudinalmente. |
| Bazo | Una sección transversal de 0,5 cm de ancho. |
| Timo | Una sección transversal de 0,5 cm de ancho. |
| Pulmón | Varias secciones, incluyendo todos los lóbulos, lesionados o no (normalmente se toman muestras de lóbulo apical, lóbulo medio y parte craneal del lóbulo diafragmático). |
| Hígado | Varias secciones de 0,5 cm de ancho. |
| Riñón | Una sección transversal de 0,5 cm de ancho. |
*Las muestras se fijan por inmersión en formol al 10%
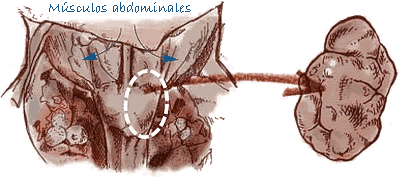 Toma de muestras de nódulos linfáticos |
||
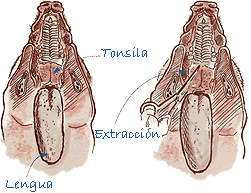 Toma de muestras de tonsila |
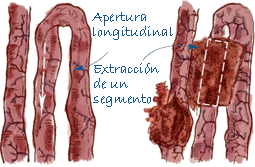 Toma de muestras de íleon |
|
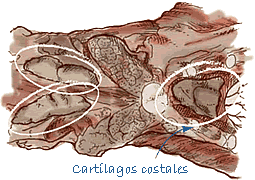 Toma de muestras del timo |
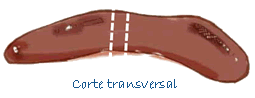 Toma de muestras del bazo |
|
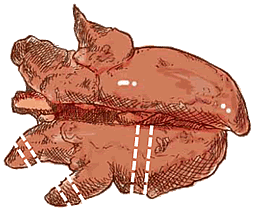 Toma de muestras de pulmón |
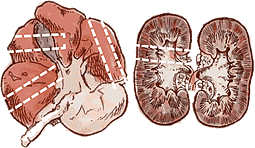 Toma de muestras de hígado y riñón |
|
 |
|
|
|
Para evitar equívocos, la solicitud a realizar para confirmar el objetivo primero es la de “estudio histopatológico y de detección de PCV2 en los tejidos”.
Para completar el segundo de los objetivos (diagnóstico global), deberían tomarse todas aquellas muestras necesarias para poder confirmar/descartar la circovirosis porcina así como todas aquellas enfermedades potenciales que hayan sido incluidas en la lista de diagnóstico diferencial. Aquí existirían dos grandes opciones: 1. Tomar estas muestras y remitirlas al laboratorio o laboratorios de diagnóstico correspondientes. 2. Enviar animales enteros, significativos del problema clínico, al laboratorio diagnóstico, indicando el diagnóstico diferencial que se pretende confirmar o descartar. En este caso, la solicitud a realizar debería incluir “estudio anatomo-patológico, histopatológico y microbiológico (bacteriológico/virológico) de las enfermedades que se incluyen en la lista de diagnóstico diferencial”. GRAN IMPORTANCIA DIAGNÓSTICA: Remítanse siempre muestras de varios animales o varios animales enteros para poder establecer el diagnóstico concreto o los diagnósticos globales que se persiguen; remitir muestras de un solo animal o un solo animal entero suele limitar en gran medida la obtención de un resultado diagnóstico útil. |
   |
|




