Pese a la disponibilidad y al uso extendido de las vacunas contra el virus de la influenza A (IAV), la enfermedad sigue siendo un lastre importante para la industria porcina. Las vacunas utilizadas en porcino suelen estar formadas por virus enteros inactivados (WIV) que contienen un adyuvante del tipo aceite en agua y se suelen administrar por vía intramuscular. Se han explorado otros sistemas y en Estados Unidos existe una vacuna de subunidades que contiene una partícula de ARN no replicante de alfavirus que codifica para el gen HA. Además, las granjas pueden desarrollar sus propias autovacunas. Normalmente la vacunación se lleva a cabo en las cerdas para generar anticuerpos maternales que sean transferidos a sus camadas vía calostro, aunque ocasionalmente también se vacunan los cerdos de engorde. Pese a que hay varias vacunas completamente autorizadas, no se actualizan con la misma rapidez con la que el virus evoluciona antigénicamente. Esto puede generar una protección subóptima contra cepas antigénicamente distintas.
Para que una vacuna sea autorizada, debe demostrar que es segura y eficaz. Para cumplir con los requisitos de eficacia, los fabricantes deben demostrar la inmunogenicidad de la formulación mediante inhibición de la hemaglutinación (HI) y/o reducción de los títulos víricos en los pulmones de cerdos vacunados desafiados experimentalmente con una cepa homóloga a la del virus vacunal. El tiempo requerido para modificar la formulación de una vacuna que ya está aprobada varía según la legislación del país, y esto dificulta las actualizaciones que serían necesarias para adaptar la vacuna a la rápida evolución del virus. Sin embargo, cambios recientes de la legislación llevados a cabo por el Centro de biología veterinaria del USDA (EEUU) podrían reducir este tiempo en el futuro.

En un contexto de campo, la eficacia vacunal debe tener en cuenta cada explotación de forma individual y el resultado deseado. El test de HI, el estándar para la caracterización antigénica, suele estar correlacionado con los títulos de neutralización vírica por lo que se utiliza para inferir la protección. Normalmente se considera que un título recíproco de 40 o superior es protector, sin embargo, los títulos séricos de HI no siempre están bien correlacionados con la eficacia y la protección vacunal; en algunos casos ni siquiera frente a las mismas cepas si ciertos factores interfieren en el momento en que se administra la vacuna.
Conseguir la autorización de una vacuna es un proceso laborioso, caro y que puede ser considerablemente largo. Idealmente, las actualizaciones en la formulación de las vacunas porcinas frente a IAV podrían seguir un proceso similar al que se lleva a cabo con la selección de cepas para adaptar las vacunas humanas a la estacionalidad anual, basándose en la vigilancia e identificación nacional o regional de nuevas cepas antigénicamente distintas (figura 1). El desafío radica en que la evolución genética y antigénica del virus de la influenza porcina es mucho más dinámico que en los virus humanos, con una variación substancial entre distintas regiones geográficas e incluso con la cocirculación de muchas cepas distintas en una misma región (Vincent et al., 2014).
La toma de decisiones sobre las vacunas se basa en la vigilancia y la monitorización de las cepas circulantes de IAV (figura 1). Los primeros pasos para desarrollar un programa de selección de vacunas más dinámico y actualizado son analizar las secuencias disponibles de los virus porcinos circulantes y las posiciones antigénicas conocidas en la secuencia de aminoácidos de HA. Desgraciadamente, la similitud de la secuencia de aminoácidos (y, en menor medida, la similitud de nucleótidos) no siempre es indicativa de protección cruzada. En los virus porcinos H3, los grandes cambios antigénicos se producen en seis posiciones de aminoácidos cerca del receptor de HA e incluso la substitución de un solo aminoácido tiene un impacto significativo sobre la antigenicidad (Lewis et al., 2014). Por el contrario, los virus porcinos H1, tienen una diversidad genética más compleja, posiblemente como resultado de su evolución a partir de virus clásicos y de la repetida introducción de virus humanos en los cerdos durante un largo periodo de tiempo. Como consecuencia los cambios antigénicos no han sido atribuidos a mutaciones de un único aminoácido dentro de las hemaglutininas H1, aunque la sustitución de un único aminoácido en, o cerca, del receptor tiene un importante efecto acumulativo sobre la antigenicidad. Por lo tanto, la caracterización antigénica es un paso crucial que debe ser utilizado en combinación con la secuenciación y la información epidemiológica para tener más información en la toma decisiones (figura 1).
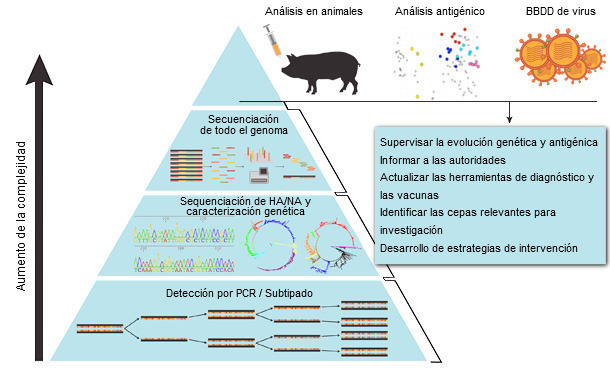
Figura 1. Método sistemático de vigilancia del virus de la influenza A en porcino (basado en Ampofo et al., 2015).
Bajo las circunstancias ideales, la respuesta inmune generada con vacuna inactivada es suficiente para reducir los signos clínicos y los títulos virales en pulmón tras la infección, siempre que ésta sea producida por un virus muy similar antigénicamente. Sin embargo, las vacunas inactivadas a menudo no bloquean completamente la infección en condiciones de campo normales. Los anticuerpos maternales generados a partir de la vacunación de las cerdas pueden proteger a los lechones contra los signos clínicos, pero no contra la infección, y pueden ser detectados hasta las 14 semanas de edad (Loeffen et al., 2003). Un efecto negativo de dichos anticuerpos es que pueden interferir con la eficacia vacunal y con la respuesta inmune activa de los lechones vacunados. De hecho la inmunidad previa, ya sea pasiva o adquirida, puede interferir con la respuesta inmune frente a vacunas muertas.
Es improbable que los anticuerpos estimulados por las vacunas inactivadas o los adquiridos por transferencia pasiva proporcionen una protección cruzada completa contra la infección con un virus distinto, lo que conlleva un fallo vacunal y más gastos para los productores. El fallo vacunal puede complicarse todavía más si la vacunación induce anticuerpos de reacción cruzada frente a un HA del mismo subtipo que impida la neutralización en una infección posterior (es decir, sin reactividad cruzada en el test HI) lo que puede acabar produciendo la enfermedad respiratoria agravada asociada a la vacuna (VAERD;(Gauger et al., 2011)). Para que se produzca la VAERD, es necesario que los HA y NA entre el virus de la vacuna y el infectivo no coincidan. Se ha demostrado VAERD en muchos escenarios experimentales y hay indicios de que se produce en el campo.
Las limitaciones de las vacunas inactivadas para generar una protección cruzada contra virus antigénicamente diferentes evidencian la necesidad de desarrollar vacunas que tengan una protección cruzada más amplia. Se han evaluado varias plataformas vacunales para IAV en porcino y todas han tenido sus pros y sus contras (figura 2). Las vacunas vivas atenuadas IAV (LAIV) han demostrado ser seguras en condiciones experimentales y más eficaces contra virus antigénicamente distintos (figura 2), reduciendo la transmisión viral y superando la interferencia de los anticuerpos maternales (Pena et al., 2011; Vincent et al., 2012). Las vacunas de subunidades y las vacunas RNA o DNA basadas en HA y NA también han demostrado que protegen contra la infección, con la ventaja de que con esta nueva tecnología es relativamente fácil modificar la formulación de la vacuna para tener en cuenta la diversidad antigénica y la aparición de nuevos virus (Wesley et al., 2004). Se seguirán explorando nuevas plataformas vacunales como alternativa a las vacunas inactivadas.
 Inactivada |
 |
 Atenuada |
|
| Vía de administración | intramuscular | intramuscular/intranasal | intranasal |
| Respuesta HI | +++ | ++ | + |
| Células secretoras de anticuerpos | ++ | + | + |
| Células B de memoria | + | + | + |
| IgA nasal | -/+ | -/+ | +++ |
| Anticuerpo NA | +++ | -/+ | ++ |
| Células CD4 T | ++ | ++ | +++ |
| Células CD8 T | - | + | + |
| Inmunidad cruzada | -/+ | + | ++ |
| Enfermedad respiratoria agravada asociada a la vacuna (VAERD) |
yes | -/+ | no |
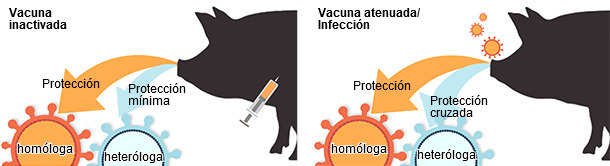
Figura 2. Eficacia comparativa de diversa plataformas vacunales frente a la infección por el virus de la influenza A en cerdos
(basado en Sridhar et al., 2015).
La estrategia vacunal debe planificarse para cada caso concreto, según las circunstancias. Las vacunas inactivadas pueden ser eficaces si se utilizan en combinación con otras prácticas, como un movimiento controlado de los animales y personas y con un análisis cuidadoso de si el antígeno vacunal coincide con el de la cepa circulante. Es necesario saber qué cepas están circulando en cada granja. La gripe porcina es una enfermedad dinámica que evoluciona continuamente, por lo que las estrategias de monitorización y control tienen que ser intensas y adaptables.



