Certificación en producción libre de antibióticos (PLA), desde el destete hasta el sacrificio en porcino
24-jul-2018 (hace 6 años 8 meses 7 días)
Ante el desafío actual, con la proliferación de bacterias multirresistentes a los antibióticos y la necesidad de reducir el consumo de antibióticos en producción porcina, desde el Grupo Térvalis (Teruel), y en una de sus empresas de producción (Terraibérica Desarrollo) se inició un proyecto en junio de 2015, para la producción y comercialización de cerdos que no reciben ningún antibiótico a partir del destete.
Esta iniciativa fue inicialmente desarrollada y certificada (septiembre 2016) mediante pliego privado, y en abril 2017 se cedió a AENOR, para convertirla en certificación abierta (accesible a cualquier empresa), siendo la primera de este tipo en Europa.
El desarrollo de este proyecto abarca diferentes campos:
- Producción ganadera: registros y trazabilidad de todos los lotes de animales, e implementación de buenas prácticas y formación del personal.
- Fabricación de piensos: trazabilidad de los piensos libres de antibióticos y límites estrictos de contaminación cruzada.
- Empresas del sector cárnico: implementación de sistemas de registros para la trazabilidad hasta el producto final comercializado.
- Centros de investigación y de desarrollo científico, donde se han establecido acuerdos marco para colaboración en investigación de nutracéuticos (fitobióticos), para optimizar y potenciar las siguientes actividades: antioxidante, antimicrobiana (bactericida y/o antiparasitaria), antiinflamatoria e inmunoreguladora.
Las bases técnicas para conseguir y preservar las condiciones de una producción libre de antibióticos se establecen según las siguientes pautas:
- Valoración inicial del estatus sanitario y nivel de bioseguridad en la zona y en la explotación: densidad granjas, desinfección, vacíos sanitarios…
- Comprobación de dimensionamientos y estructura de la granja para optimizar el espacio por animal y el acceso a comedero y bebedero.
- Formación, concienciación e implicación del personal: motivación.
- Aplicación rigurosa de los programas vacunales.
- Verificaciones analíticas frecuentes (3-4 veces / año).
- Programas de alimentación formulados específicamente para buscar estabilidad digestiva: perfiles adecuados de fibra dietética, digestibilidad proteica, minimizar cloruros, etc.
- Programa de manejo de los piensos en multifase (7 a 8 piensos desde destete a sacrificio), “choice feeding”, …
- Utilización de nutracéuticos formulados a base de extractos cítricos y de aliáceas.
Desarrollo en investigación
El grupo Térvalis dispone de departamento de I+D+i, apoyado en acuerdos con centros de investigación externos, para la aplicación en producción ganadera de extractos vegetales propios, a base de cítricos y aliáceas.
Tanto los extractos cítricos como los extractos de aliáceas, así como cualquier otro principio activo candidato a ser utilizado, se someten a pruebas de eficacia. Algunos de los trabajos y técnicas llevadas a cabo por DIGESPORC (Facultad de Veterinaria de León), han sido:
1.- Concentración mínima inhibitoria (MIC) y concentración mínima bactericida (MBC).
| Cepa | MIC | MBC | |
| EC58 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC59 | Escherichia coli (cepa hemolítica) | 64 | 64 |
| EC60 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC61 | Escherichia coli (cepa hemolítica) | 64 | 64 |
| EC62 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC63 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC64 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC65 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| EC66 | Escherichia coli (cepa hemolítica) | 64 | 64 |
| EC67 | Escherichia coli (cepa hemolítica) | 128 | 128 |
| 8766 | Campylobacter coli | 32 | 32 |
| 10131 | Campylobacter coli | 32 | 32 |
| 10604 | Campylobacter coli | 32 | 32 |
| 10647 | Campylobacter coli | 32 | 32 |
| DSMZ4688T | Campylobacter jejuni | 32 | 32 |
| 6937 | Campylobacter jejuni | 32 | 32 |
| 7672 | Campylobacter jejuni | 32 | 32 |
| 7674 | Campylobacter jejuni | 32 | 32 |
| 34 | Campylobacter upsaliensis | 32 | 32 |
| 60 | Campylobacter upsaliensis | 32 | 32 |
2.- Inhibición de biofilms.
3.- Cinética de inactivación de los diferentes patógenos estudiados.
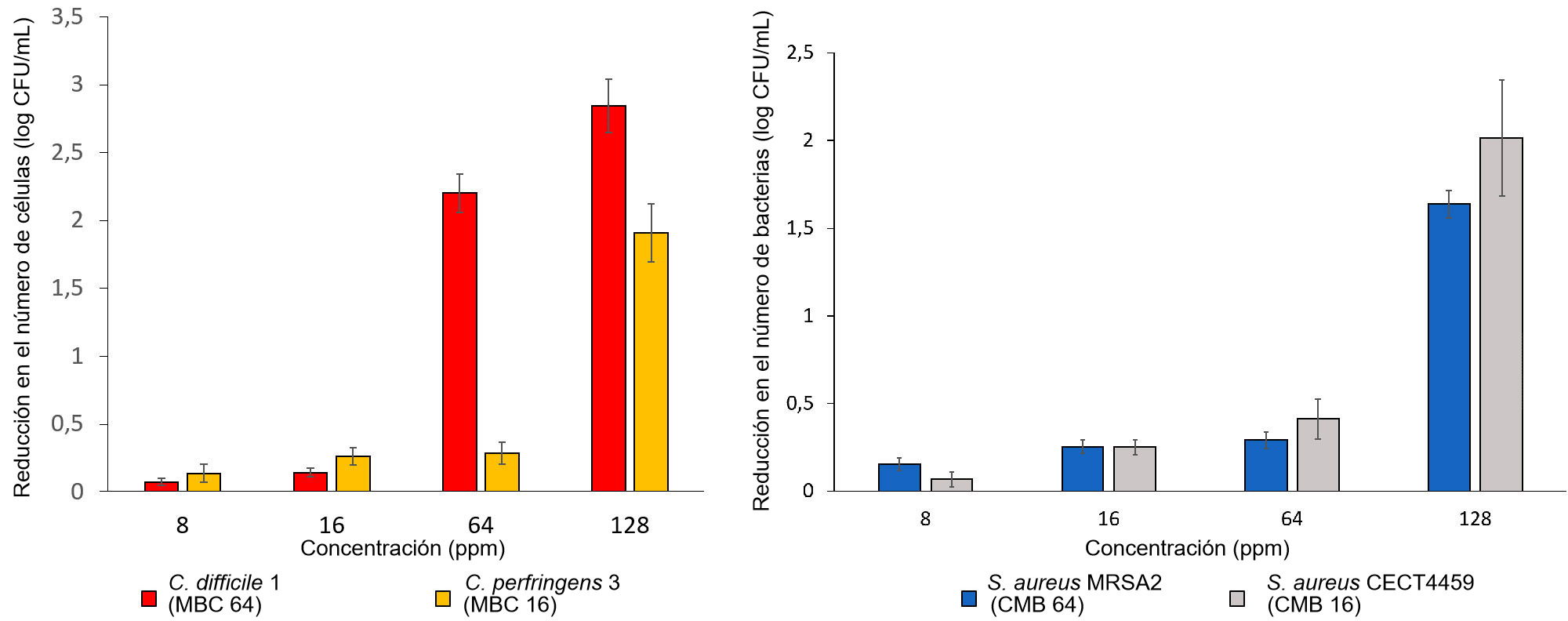
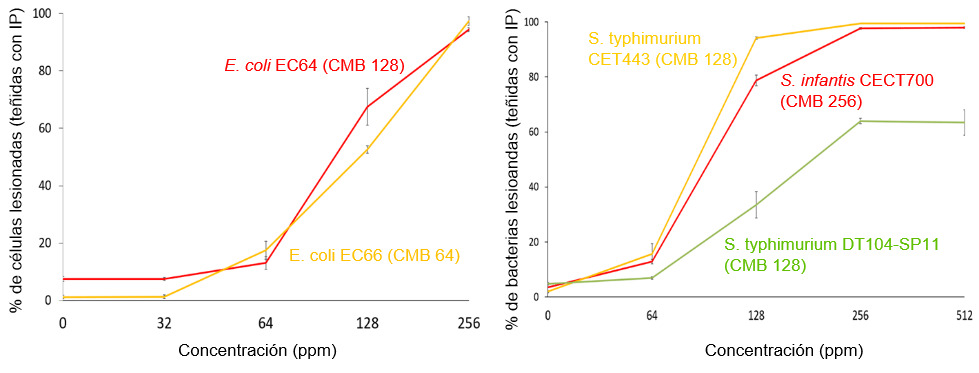
4.- Test de integridad de la membrana bacteriana por citometría de flujo.
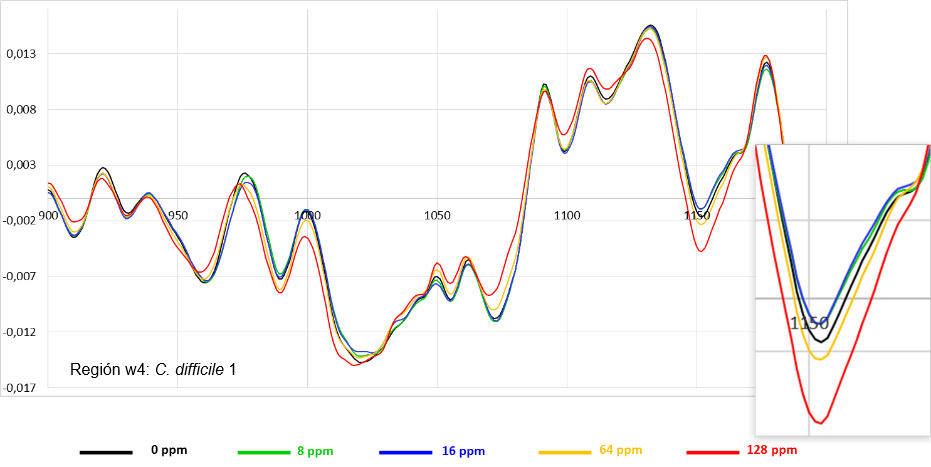
5.- Análisis espectroscópico infrarrojo por transformada de Fourier (FTIR).
6.- Microscopía electrónica de barrido.
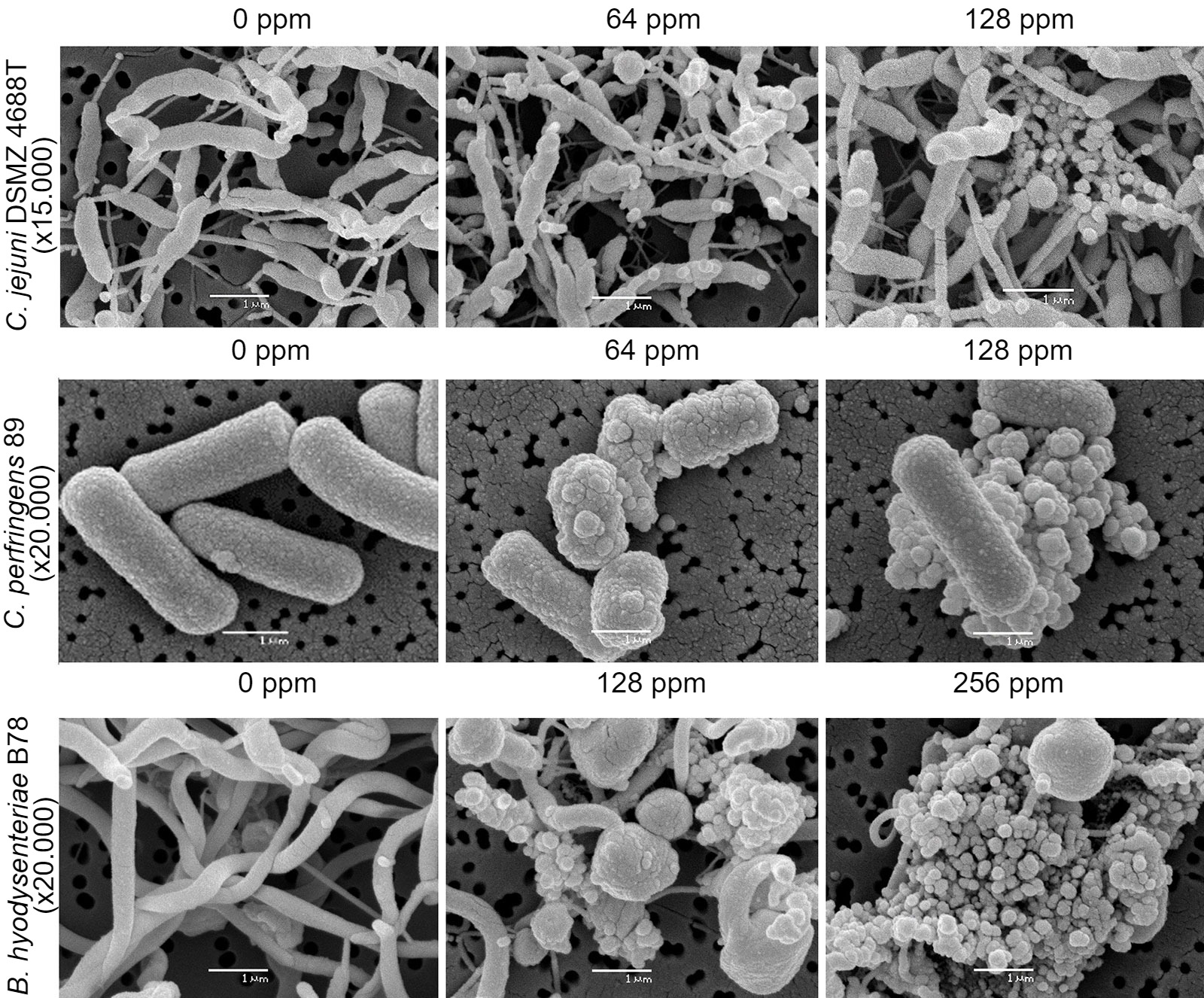
Las evaluaciones de actividad antimicrobiana se llevan a cabo sobre los principales patógenos digestivos (E. coli, C. perfringens y C. difficile, diversos serovares de Salmonella, Campylobacter coli y C. jejuni, y B. hyodysenteriae) así como en S. aureus resistentes a meticilina (MRSA).
Estos estudios han sido publicados en diversas publicaciones técnicas.
Tras su evaluación, los productos desarrollados para su aplicación en condiciones de campo, tienen como base en su formulación, la combinación de los extractos cítricos y de aliáceas, incorporados en diferentes proporciones, y/o con otros principios activos y materias primas, según lo requiera la fase de producción, el nivel de desafío y los objetivos a conseguir que podemos clasificar en:
- Objetivos metabólicos, para la mejora de eficacia nutricional de los piensos, y corrección de desequilibrios fisiológicos en cerdas, lechones y engordes.
- Objetivos en salud intestinal, para conseguir estabilidad en la microbiota, actuando como potenciadores de bacterias simbióticas beneficiosas, y acción antimicrobiana frente a patógenos digestivos.
Desarrollo en condiciones de campo
CONTROL EN GRANJA Y FABRICA DE PIENSOS
- Se certifica que no hay aplicación ni tratamiento profiláctico o metafiláctico con antibióticos, quedando excluida por completo la medicación en pienso y/o agua. Se identifican los animales con síntomas iniciales de enfermedad, y tras el diagnóstico correspondiente, se aplica tratamiento antibiótico específico (solo inyectable y/o tópico).
- Durante la fabricación de piensos para otras explotaciones de porcino no adscritas a la certificación, se aplica un protocolo para minimizar la posibilidad de contaminación cruzada, estableciéndose un orden de fabricación según una clasificación de los piensos en: nunca medicados, eventualmente medicados, y probablemente medicados.
- Se audita periódicamente el cumplimiento de unos estrictos límites de trazas (ppb) de antibióticos en pienso (fábrica, silos y tolvas) y en el agua de bebida.
- Se establece un acuerdo firmado con los proveedores de antibióticos para que mensualmente envíen un listado con el consumo de antibióticos por lote y granja.
- Periódicamente se hace un balance de masas en el stock, consumo y aplicación de antibióticos inyectables y/o uso tópico.
- Registro permanentemente de los tratamientos antibióticos (inyectables y/o tópicos) llevados a cabo, mediante los datos recogidos en el sistema de identificación con crotal electrónico: identificación del animal, lote de producción, antibiótico utilizado, día de aplicación y duración de tratamiento. Los cerdos tratados pasan a ser de producción convencional.
CONTROL EN MATADERO
- Con la entrada a matadero se identifica el número de animales PLA y animales de producción convencional (identificados con crotal electrónico), mediante albaranes y guías independientes según el tipo de producción.
- Periódicamente se audita en los mataderos, salas de despiece e industrias de elaboración el mantenimiento de la cadena de custodia y la trazabilidad.
Se realiza una gestión coordinada donde se comunican los resultados obtenidos, cumplimiento de la certificación y resultado en las auditorías a todos los involucrados en la cadena de producción.
Resultados
Los resultados finales de la aplicación de todas las medidas descritas anteriormente a los diferentes niveles de la producción han permitido:
- Producir un 96,3% de animales libres de antibióticos desde el destete.
- Cerdas reproductoras: no medicadas con antibióticos, ni en pienso ni en agua en los últimos 32 meses (último tratamiento en octubre de 2015). Los tratamientos antibióticos en reproductoras se han reducido a la mínima expresión y siempre como tratamientos individuales. Este grupo podría ser tratado al no entrar en las exigencias de la certificación.
- Tratamientos antiparasitarios: tras los análisis pertinentes que se realizan trimestralmente no ha sido necesario tratamiento en el pienso en ninguna fase de la producción (cerdas, lechones y engorde), con el último tratamiento llevado a cabo en (blanqueo y desparasitación en junio de 2015). Este tipo de tratamiento estaría permitido, ya que no entra en las exigencias de la certificación.
- Consumo en mg de antibióticos por PCU. Este ratio se calcula trimestralmente, y la totalidad de los antibióticos utilizados corresponde a los administrados por vía inyectable y/o tópica (no ha habido consumo vía pienso y/o agua desde febrero de 2016). El resultado obtenido de manera continuada desde el 2º trimestre de 2016 hasta el primer trimestre de 2018, oscila de 2 a 3 mg/PCU. En el último trimestre el resultado ha sido de 2,62 mg / PCU anuales.
