Control de Actinobacillus pleuropneumoniae (II): infección crónica
07-jun-2016 (hace 8 años 9 meses 24 días)
El objetivo de este segundo artículo es analizar las implicaciones de las infecciones crónicas por Actinobacillus pleuropneumoniae (App) en una granja y cómo controlarlas.
Tras un brote primario dentro de un sitio permanentemente ocupado o uno que se llene con animales procedentes de un origen permanentemente infectado, pueden producirse distintos escenarios.
- La enfermedad desaparece sin signos clínicos ni patológicos a largo plazo.
- La infección puede disminuir pero seguir causando brotes agudos ocasionales.
- App pasa a formar parte de la "sopa" que causa el complejo respiratorio porcino junto con otros agentes, especialmente Mycoplasma hyopneumoniae y PRRS. Esto es más probable en granjas con un nivel sanitario bajo o en sistemas de producción continua, a menudo con densidades elevadas, mezcla de edades y problemas de ventilación.
- La enfermedad crónica se produce a nivel individual y de forma más generalizada. Normalmente sucede en cerdos de engorde, de más de 10 semanas de vida y se suele presentar con algunos cerdos que "no van bien", una cierta tos de fondo en la granja, tasas de crecimiento reducidas y mortalidad elevada. En el matadero se observa una pleuritis fibrinosa crónica, junto con lesiones de pleuroneumonia necrotizante crónica. Este escenario es típico de grandes poblaciones (de, por ejemplo, más de 1.000 cerdas).

Figura 1. Pleuritis fibrinosa tras una exposición a App.
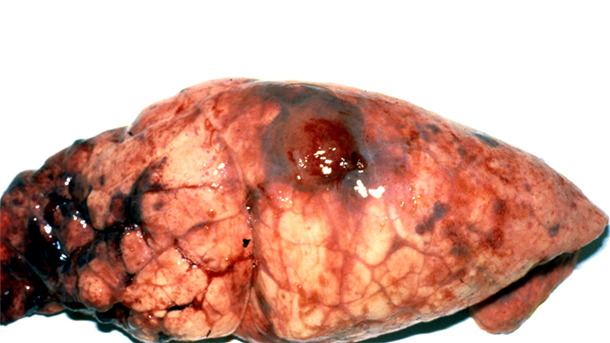
Figura 2. Lesión típica de App – la lesión pulmonar hemorrágica y necrótica está cubierta por una adherencia pleural.
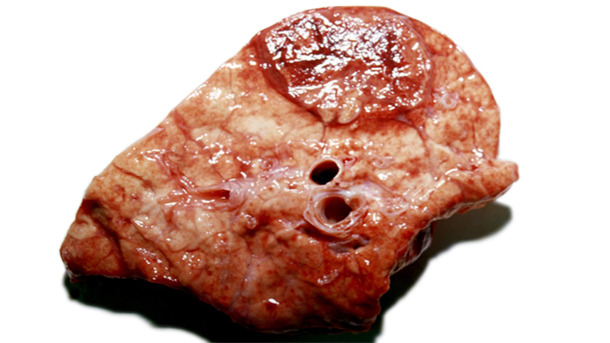
Figura 3. Sección de una lesión similar.
La epidemiología de la App crónica se debe a un ciclo de infección que empieza cuando la inmunidad maternal de las cerdas se reduce, lo que permite la infección de los lechones a partir de las 9-10 semanas de vida, la replicación y la excreción de la bacteria, la reinfección de los lechones más jóvenes y un desplazamiento de la infección, y de la inmunidad, hacia las cerdas. Los principios de control se basan en romper el ciclo a la vez que se elimina la fuente de infección de las reproductoras que, a menudo, son animales portadores asintomáticos y en reducir el paso de la infección entre grupos de edad.
Las estrategias de control dependen del sistema de manejo de cada granja, siendo un manejo de partos por bandas, con producción en sitios separados y un flujo "todo dentro/todo fuera" el que ofrece mejores oportunidades para el control. El mayor desafío lo representan los ciclos cerrados grandes y continuamente ocupados. También habrá que tomar la decisión de si se decide eliminar la enfermedad o sólo controlarla.
La mejor manera de conseguir la eliminación es mediante la despoblación total, la limpieza y desinfección y la entrada de animales libres de la enfermedad. El test serológico APXIV proporciona unos resultados más fiables que los antiguos tests de fijación del complemento para serotipos específicos, aunque la evaluación de si una granja está libre de la enfermedad todavía se basa fundamentalmente en la ausencia de signos clínico-patológicos. También puede conseguirse la eliminación por despoblación parcial con medicación. El cambio de sitio de los lechones al destete, acompañado de un tratamiento con antibióticos como la tulatromicina, ceftiofur o fluorquinolonas (sujeto a un uso responsable) tanto en cerdas como en lechones ha tenido éxito, así como el tratamiento prolongado de las cerdas con tilmicosina en pienso acompañando los tratamientos de lechones. Si se hacen lotes de parto, o se realiza una parada en el flujo de partos, es más probable que los programas tengan éxito. (Pueden combinarse con técnicas de vacunación masiva y el cierre a la entrada de reposición para conseguir la eliminación simultánea de diversas enfermedades). No se ha demostrado que sea posible eliminar activamente App de ciclos cerrados afectados crónicamente si están permanentemente ocupados.
Si hay aspectos geográficos, económicos o prácticos que impidan la eliminación de la enfermedad, deben utilizarse medidas de control a largo plazo. El tratamiento antimicrobiano en las fases de máximo riesgo es el método más simple y, si podemos preverlo, la administración durante, por ejemplo, dos semanas de pienso medicado con tilmicosina o la inyección individual con tulatromicina puede ser muy efectiva para suprimir la enfermedad, y reducir las lesiones en matadero. Alternativamente puede utilizarse medicación en agua durante 5 días de un modo metafiláctico, especialmente cuando los animales se acercan al peso de matadero y deban utilizarse productos con un periodo de supresión más corto. En situaciones extremas en las que la enfermedad aparece repetidamente antes del matadero, se utilizan antibióticos con un periodo de retirada corto, como la tiamulina en pienso o agua, pero la medicación antibiótica profiláctica a largo plazo, o permanente, ya no se considera aceptable.
El control mediante la vacunación ha demostrado ser fiable ya sea mediante el uso de vacunas comerciales o autógenas, preparadas a partir del aislado específico de la granja. Estos productos son una solución cara y a largo plazo y debe considerarse su efecto sobre la epidemiología dentro de la explotación. Normalmente si la vacuna se administra a las, digamos, 9 y 12 semanas en una granja de ciclo cerrado, el efecto de la reducción de la enfermedad en el engorde puede reducir la presión "hacia atrás" sobre las cerdas, lo que implica una reducción de los anticuerpos maternales. La enfermedad puede avanzar hacia atrás y afectar progresivamente a los lechones más jóvenes. Esta situación dinámica requiere un reajuste contínuo del programa vacunal y puede requerir, en último término, la vacunación tanto de las cerdas como de los cerdos de engorde para mantener la estabilidad.
Si las vacunas comerciales se basan en toxinas APX y proteínas de membrana, ya no es necesario –a no ser que tenga un propósito epidemiológico– serotipar la cepa antes de introducir el programa vacunal.
