Manejo estratégico de las cerdas de reemplazo para un control de PRRS sostenible
15-ene-2013 (hace 12 años 2 meses 16 días)
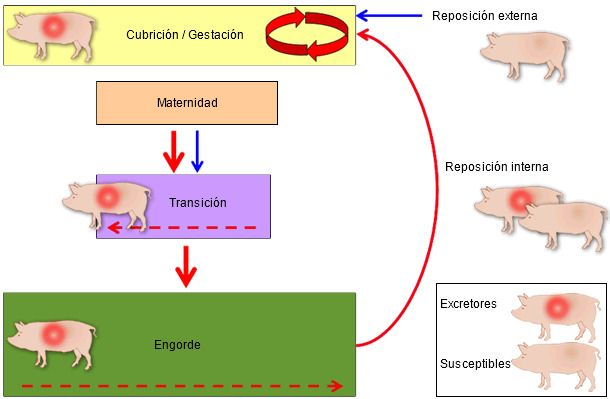
Tras la introducción del virus de PRRS en una granja de reproducción, es frecuente observar fallo reproductivo y aumento de la mortalidad (Loula, 1991). En unos cuantos meses, los parámetros reproductivos pueden volver a valores similares a los de antes de la infección; sin embargo, la coexistencia de subpoblaciones infectadas y susceptibles perpetúa la transmisión viral dentro de la explotación (Dee et al., 1996). El virus puede replicarse tanto en nulíparas negativas como en las previamente infectadas si se hallan mezcladas con individuos excretores (Figura 1). Esta dinámica provoca el destete continuo de lechones infectados que suelen estar clínicamente afectados tras la mezcla y la caída de la inmunidad maternal. Las transiciones con una infección activa representan un riesgo de infección para las maternidades de origen y las granjas vecinas. Los estudios económicos indican que la mayor parte del coste asociado a PRRS se produce en los lechones de transición y no en las cerdas (Neumann et al., 2005; Holtkamp et al., 2011).
Figura 1. Mecanismo de perpetuación de la infección por PRRSV en una reproducción
En países donde se ha alcanzado un consenso sobre el impacto económico de la enfermedad, el objetivo estándar para el control de PRRS es la producción consistente de lechones destetados negativos. La American Association of Swine Veterinarians activó un comité liderado por los Drs Holtkamp y Polson en 2011 para desarrollar una terminología estandarizada para clasificar las explotaciones según su grado de infección por el PRRSV. La clasificación describe recomendaciones de testeo para definir las explotaciones desde Positivas (categoría I) a Negativas (categoría IV) durante el proceso de estabilización o eliminación. Una explotación se describe como estable (categoría II) cuando las muestras de suero de al menos 30 lechones antes del destete, analizadas mediante PCR en grupos de cinco, son negativas en cuatro muestreos mensuales consecutivos (120 muestras de suero = 24 test de PCR distribuidos homogéneamente durante 90 días). Una vez que el hato está estabilizado, las nulíparas negativas a ELISA pueden mezclarse con la población previamente infectada con relativamente poco riesgo de infección. Si 60 nulíparas son negativas mediante un ELISA individual dos meses después de su introducción en la población, puede definirse la explotación como Provisionalmente Negativa (categoría III). Cuando todas las cerdas originalmente infectadas (ELISA positivas) han sido reemplazadas (“rolled-over”) por nulíparas ELISA-negativas sin evidencia de infección, la explotación puede clasificarse como Negativa (categoría IV).
Para eliminar el PRRSV de las explotaciones se ha propuesto el método de despoblación de cerdos infectados y repoblación con cerdos negativos, y el de "análisis y eliminación"; sin embargo, el procedimiento más rentable para eliminar el virus es el cierre de la granja o llenado-cierre-homogenización, LCH (Yeske, 2011). El protocolo se aplica a reproducciones infectadas de forma aguda o endémica y normalmente empieza con la introducción de tantas nulíparas como las instalaciones puedan albergar (Llenado), a continuación se interrumpe la reposición interna o externa de hembras o machos hasta que la explotación pueda definirse como estable (Cierre). Finalmente se lleva a cabo la exposición simultánea de todos los individuos adultos al virus residente de PRRS o a la vacuna del virus vivo modificado (Homogenización), este último punto se realiza una o dos veces. Una variación llamada reposición externa (“off-site breeding”), consiste en tener una instalación separada donde se crían y cubren la cerditas de reposición negativas, que sólo serán movidas a la reproducción cuando se haya confirmado la estabilidad, o las cerditas puedan infectarse con la misma cepa utilizada para homogenizar la reproducción, exactamente en el mismo momento. Los protocolos de bioseguridad y monitoreo son críticos para asegurar la introducción de PRRSV en estas nulíparas.
Figura 2. Ejemplo de procedimientos y detección de PRRSV en lechones al destete durante el cierre de la explotación
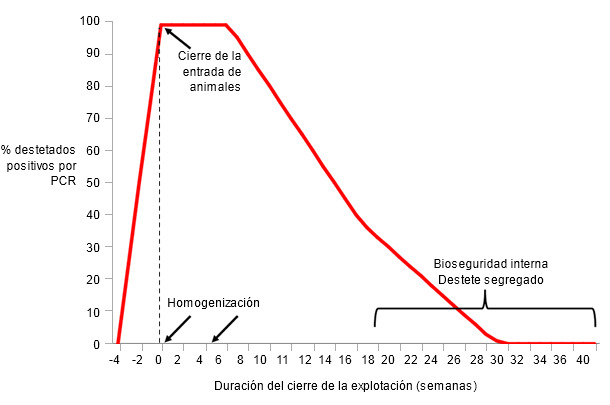
La proporción de lechones positivos por PCR al destete empieza a decaer unas semanas después de la homogenización (Figura 2). En algún momento durante el cierre, probablemente tras 16 semanas, los cerdos nacen no virémicos pero se infectan durante la lactación con un ratio muy bajo (Cano et al., 2008). Por lo tanto la bioseguridad interna para minimizar la transmisión en las salas de maternidad y una segregación efectiva de los lechones destetados son críticas para completar la eliminación de PRRSV de la explotación. Un estudio reciente de la Universidad de Minesota reveló que, desde el momento del cierre, las explotaciones tardan unas 30 semanas (12 a 43 semanas) para destetar lechones PCR-negativos de un modo consistente. Los autores encontraron que el método de exposición al virus y el grado de infección previa afectaban significativamente al tiempo necesario para estabilizarse (Linhares et al., 2012).
Con protocolos ligeramente distintos, los veterinarios de Norteamérica confían en los métodos actuales para eliminar el PRRSV de una explotación; Sin embargo, la pregunta del millón es qué hacer con las nulíparas una vez eliminado el virus.
“¿La reposición debe ser negativa, vacunada o debe infectarse con virus residente?”.
La decisión sobre la aclimatación de la reposición para PRRS puede ser excesivamente simplista en base al riesgo de una nueva infección en la reproducción. Si se asume que este riesgo está en función de la densidad de cerdos local, la prevalencia de PRRSV de la zona y el nivel de bioseguridad de la granja, pueden proponerse tres situaciones e intervenciones potenciales:
| Riesgo | Bajo | Medio | Alto |
| Densidad local y prevalencia de PRRS | Muy baja | Baja-media | Medio-alta |
| Infraestructuras de bioseguridad y protocolos | Excelentes | Aceptables | Pobres |
| Frecuencia esperada de brotes de PRRS | Rara | Cada 2 o 3 años | Cada año o más |
| Grado de infección de PRRS de la empresa | Negativo | Negativo-estable | Estable-Positivo |
| Objetivo de producción | Multiplicador externo | Multiplicador interno o comercial | Comercial |
| Plan de acción tras un brote de PRRS | Eliminación | Estabilización | Control |
| Diagnóstico de PRRS en lechones destetados | PCR/ELISA-negativo | PCR-negativo | PCR-negativo/positivo |
| PRRS en la reposición externa/semen | Negativo | Negativo | Negativo |
| Período de cuarentena de la reposición (semanas) | 6 | 3 | 2 |
| Inmunización de las nulíparas (aclimatación) | No | Virus vivo-modificado y/o vivo-residente | Virus vivo-modificado |
| Recuperación de las nulíparas (“cooling”) (semanas) | No | 14 | No |
En las explotaciones situadas en zonas con poca densidad y/o poca prevalencia y con una bioseguridad adecuada, la eliminación de PRRSV está indicada. Cuando la introducción de la enfermedad ha sido esporádica y el objetivo es producir cerdos negativos, la reposición puede ser negativa y monitorizarse mediante un programa de vigilancia exhaustivo. Por otro lado, debido a que las consecuencias de un brote de PRRS en una explotación negativa suelen ser significativamente más elevadas que en las de una explotación previamente expuesta, la inmunización de las cerdas de reemplazo en explotaciones con riesgo moderado-alto es muy recomendable. Pese a la falta de conocimiento sobre una protección heteróloga completa en las reproducciones y la dificultad para predecir la próxima cepa de PRRSV, estudios recientes muestran que la inmunidad previa no sólo reduce el tiempo necesario para alcanzar la estabilidad sino también el necesario para recuperar el nivel de productividad previo a la infección y minimizar las pérdidas productivas durante el brote (Linhares et al., 2012).
Pese a que la exposición de las nulíparas a las cerdas viejas, lechones virémicos o tejidos, son métodos de aclimatación propuestos, la dificultad para determinar la dosis y el tiempo de infección limita seriamente el uso de dicha estrategia. La inyección del virus salvaje en las cerditas de reposición es una práctica habitual, igual que el uso de vacunas vivas modificadas. La severidad de los signos clínicos y la capacidad del proceso para conseguir una exposición efectiva pero evitando la entrada de cerditas que estén eliminando virus a la reproducción tiene que ser valorada para decidir entre el virus vivo-modificado y el salvaje. La fase de recuperación del periodo de aclimatación en una maternidad estable tiene que ser de, al menos, 100 días en grupos todo dentro/todo fuera para evitar la recirculación del virus. Cuando el riesgo de infección es elevado la posibilidad de llevar a cabo un cierre de la explotación cada vez que entra un nuevo virus PRRS es complicada. En estos casos, la decisión más beneficiosa puede ser la maximización de la inmunidad y la minimización de la exposición mediante el uso sistemático de la vacunación de las nulíparas a la llegada y un mes después y la vacunación de los lechones al destete.
El resultado deseado del manejo estratégico de la reposición a nivel de empresa es la minimización de las pérdidas económicas potencialmente causadas por PRRS. Una medida integrada de éxito es el cálculo del número medio de semanas en las que se destetan lechones PCR-negativos por granja de reproducción en el conjunto del sistema productivo. Los cerdos negativos tienen mayores posibilidades de desarrollarse que los positivos, incluso si son trasladados a zonas de alta densidad porcina y alta prevalencia de PRRS, porque la vacunación al destete les permitirá desarrollar una inmunidad activa, normalmente, antes de cualquier exposición.
