La incidencia y el impacto de la infección por circovirus porcino tipo 2 (PCV2) y sus patologías asociadas (PCVAD, antiguamente PMWS) han cambiado considerablemente en los últimos 15-20 años. Antes de 2004, PCV2 tenía una elevada prevalencia en la población porcina pero solía ser asintomático, por lo que no había mucha confianza en el diagnóstico de las enfermedades asociadas a este agente. La definición clínica y los criterios diagnósticos del síndrome de desmedro multisistémico postdestete (PMWS, actualmente PCVAD) fueron recogidos por Sorden en 2000 (figura 1) y fueron ampliamente aceptadas por la comunidad veterinaria ya que la enfermedad se propagó por todo el mundo, pudiendo corroborarlos en la práctica. Sorden incorporó, sabiamente, los signos clínicos típicos, las lesiones típicas y la demostración del virus en la definición clínica y en los criterios diagnósticos.
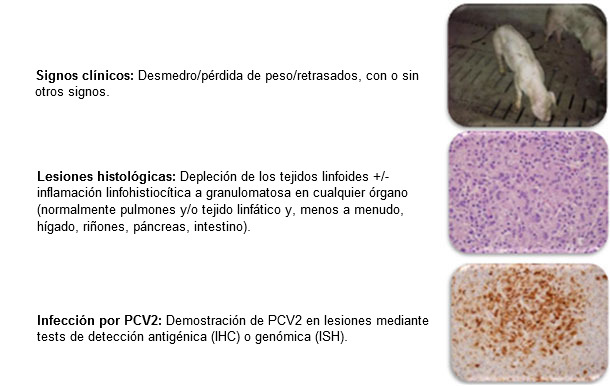
Figura 1: PMWS: Definición clínica. Sorden, Swine Health Prod 8(3):133-136, 2000

El diagnóstico de un cerdo o grupo de cerdos requiere:
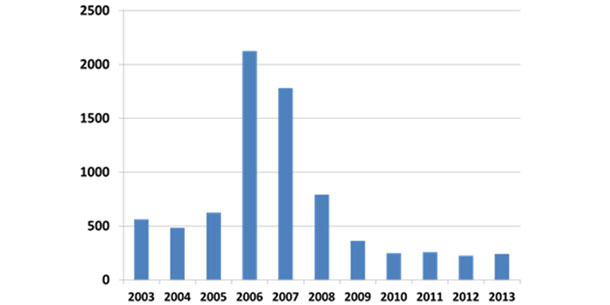
Durante la fase epidémica (2004-2007), las muertes por PCVAD en el engorde llegaban hasta el 40 %, produciendo una caída en la comercialización de casi un 10 % en EEUU. A principios de 2006, los productores pedían desesperadamente una medida efectiva. Pese a que varios grupos de investigación estaban trabajando en el desarrollo de una vacuna comercial desde finales de los 1990s, en EEUU no se comercializó ninguna hasta 2006 y no estuvo completamente disponible hasta 2007-8. Las vacunas comerciales han demostrado ser considerablemente eficaces, tanto en la prevención de las devastadoras pérdidas causadas por las muertes y el desmedro como en el aumento del rendimiento global y en la disminución de la variabilidad en la ganancia de peso. La aplicación exitosa de las vacunas comerciales ha seguido hasta la fecha; en la figura 2 se muestra la evolución del número de diagnósticos en el laboratorio de diagnóstico veterinario de la universidad de Iowa (ISU VDL).
Figura 2: Frecuencia relativa del diagnóstico de PCVAD (ISU VDL)
Las vacunas siguen siendo eficaces frente a PCVAD y casi todos los animales producidos comercialmente en EEUU están vacunados pero, debido a que PCV2 sigue circulando en las poblaciones vacunadas, en algunos casos siguen apareciendo casos de PCVAD.
Herramientas diagnósticas y variación de PCV2
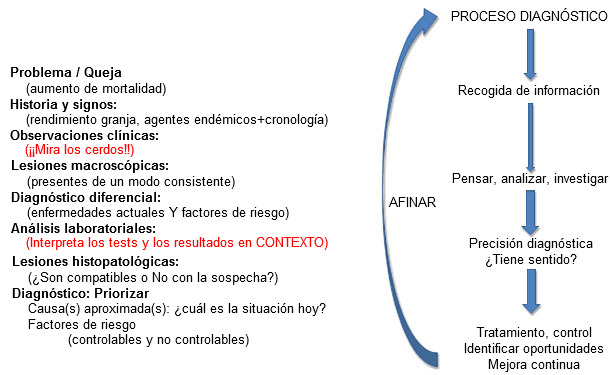
Los tests diagnósticos son herramientas que pueden ser utilizadas por profesionales con formación y experiencia en interpretarlos dentro del contexto del escenario clínico y de los hallazgos macro y microscópicos. La confianza en la exactitud de un diagnóstico requiere que todos los elementos se "alineen"- es decir, que sean precisos y expliquen una historia consistente. Las observaciones o resultados de tests que no tengan sentido deben provocar una inmediata reevaluación del proceso diagnóstico (figura 3). Es un concepto muy sencillo, pero en la práctica puede ser pasado por alto. Las suposiciones, los sesgos en las confirmaciones y la consideración superficial de las opciones diagnósticas pueden, y a menudo llevan a, producir diagnósticos erróneos.
Figura 3: "Alineamiento" diagnóstico: Toda la información debe tener sentido.
Las principales herramientas diagnósticas frente a PCVAD son:
- Histopatología con detección de antígeno o del agente en muestras de tejido (inmunohistoquímica, hibridización in situ); y
- Detección genómica (PCR) y caracterización (secuenciación) con técnicas moleculares.
La inmunohistoquímica es un método excelente para demostrar el antígeno viral en muestras de tejido con lesiones. Sin embargo, IHC no es especialmente sensible para detectar la presencia del virus y además tiene una interpretación subjetiva. Pueden darse, y se dan, resultados discrepantes. La IHC debe ser llevada a cabo por patólogos bien entrenados y, cuando no hay "alineamiento" diagnóstico, debe ser reexaminada.
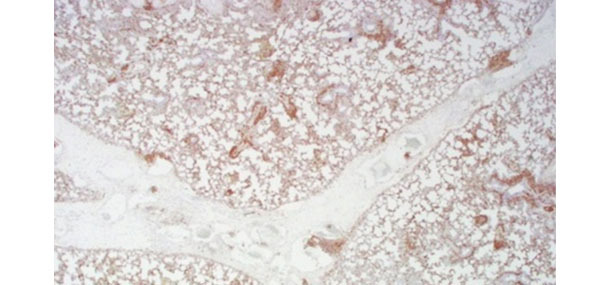
Tinción positiva (marrón) para PCV2 mediante inmunohistoquímica en pulmón
de un cerdo con edema interlobular severo y neumonía intersticial difusa.
La reacción en cadena de la polimerasa (PCR) es indudablemente el método más sensible para la detección de genes específicos. Un PCR positivo NO confirma la causa de la enfermedad – simplemente responde la pregunta "¿Hay PCV2 en la muestra analizada?" A menudo se utiliza la PCR cuantitativa o semicuantitativa en suero porcino para calcular la "carga viral". La idea de que la magnitud de la viremia o carga viral de un tejido está correlacionada con la expresión de la enfermedad y el pronóstico de la infección ha demostrado ser válida. Tras la infección con PCV2, los cerdos que no desarrollen la enfermedad clínica generarán anticuerpos neutralizantes y la viremia cesará en 3 semanas tras la infección, sin superar, probablemente, las 107 copias genómicas por mL, a menudo menos. Los cerdos afectados clínicamente suelen presentar valores más elevados y durante más tiempo. Los resultados variarán entre laboratorios por lo que es importante que los veterinarios estén familiarizados con las interpretaciones de su laboratorio.
Una de las limitaciones de la PCR es que pueden no detectarse algunas variantes del virus buscado. Esto se hizo evidentre en la investigación reciente de un nuevo PCV2b "mutante" (llamado PCV2b mutante, mPCV2b o PCV2d) que se aisló de una granja que había informado de "fallo vacunal". El ORF2 PCV2a/b diferencial que se utilizaba rutinariamente por el ISU VDL no detectó el nuevo PCV2, sin embargo, la sonda diseñada para ORF1 fue positiva. Entonces se llevó a cabo un IHC que fue positivo a PCV2 (Opriessnig). La idea de que las sondas de PCR deben actualizarse no es nueva y ha sido algo bastante común con agentes como el PRRSV. Cuando aparecen resultados que no tienen sentido, deben reevaluarse. Sin el feedback de los veterinarios clínicos más sagaces, ningún laboratorio podría estar actualizado. El impacto de la variación de cepas en el rendimiento de los tests serológicos todavía está por determinar.
La detección de anticuerpos se suele hacer mediante ELISA o técnicas de seroneutralización. Debido a la generalización de la infección, la serología ha sido de poca ayuda para el diagnóstico y sus resultados deben interpretarse con cuidado. El seroperfil de las explotaciones puede ayudar a determinar cuándo se produce la infección y también puede ser útil para evaluar el impacto potencial de los anticuerpos maternales en el momento de la(s) vacunación(es).
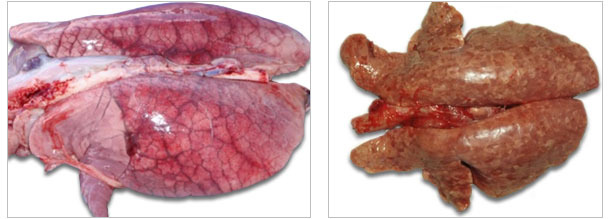
| El síndrome del edema pulmonar agudo puede observarse en PCVAD agudos. |
Pulmones oscuros y endurecidos (patrón intersticial de neumonía) de un cerdo con neumonía asociada a PCV2. |
Diagnóstico vs evaluación del impacto en la granja
El diagnóstico de PCV2 en un animal enfermo sigue siendo el mismo que Sorden describió hace 14 años. El hallazgo ocasional de un animal con PCVAD dentro de una gran población no es raro ya que la efectividad de la vacuna raramente es del 100%. Asignar automáticamente todas las variaciones del rendimiento, morbilidad o mortalidad a PCV2 basándonos en la observación de un par de cerdos sería una imprudencia teniendo en cuenta la presencia de otros patógenos endémicos (bacterias, virus, parásitos) u otros factores que puedan comprometer el rendimiento (nutrición, manejo, ambiente). Una pregunta difícil de responder es: "¿Cómo puede evaluarse el impacto de PCVAD en una población vacunada?"
Un enfoque sistemático del diagnóstico implica una monitorización cuidadosa y sistemática de los cerdos a lo largo del tiempo. A menudo, es más objetiva y provechosa la monitorización simultánea de otros agentes endémicos (Mycoplasma, PRRSV, influenza, Actinobacillus, Haemophilus, Lawsonia, Brachyspira, Salmonella, parásitos, etc) que centrarse en la simple detección de PCV2. Probablemente la mejor herramienta de diagnóstico sea la necropsia y el registro sistemático de todos los hallazgos de todos los cerdos muertos en el engorde. Pueden tomarse muestras de tejido en formalina para su examen si el diagnóstico es dudoso o quiere descartarse PCV2. La neumonía enzoñotica, la enteritis o la pleuritis crónica suelen ser causas significativas de pérdidas. Los controles rutinarios en matadero pueden mejorar el seguimiento. El seroperfil puede ayudar a identificar la fase o la edad a la que se produce la infección. El impacto de los múltiples factores identificados puede puntuarse y quizá estimarse frente a la pérdida de oportunidad total del potencial productivo. Por desgracia no se dispone aún de protocolos precisos para evaluar el impacto de PCVAD o de infecciones subclínicas por PCV2 en poblaciones.



