El pH del medio afecta a la dinámica del nitrógeno amoniacal, desplazando el equilibrio químico de este a la forma ionizada soluble (NH4+) cuando el pH es ácido, y hacia la forma no ionizada, volátil (NH3), cuando el pH es básico.

Este equilibrio depende tanto del pH como de la temperatura. En la Figura 1 se muestra el porcentaje de NH3 del total de nitrógeno amoniacal en función de estas dos variables en una disolución de nitrógeno amoniacal en agua. Aunque la salinidad de los purines puede modificar los valores indicados, estos son una buena aproximación para ilustrar lo que aquí se expone.
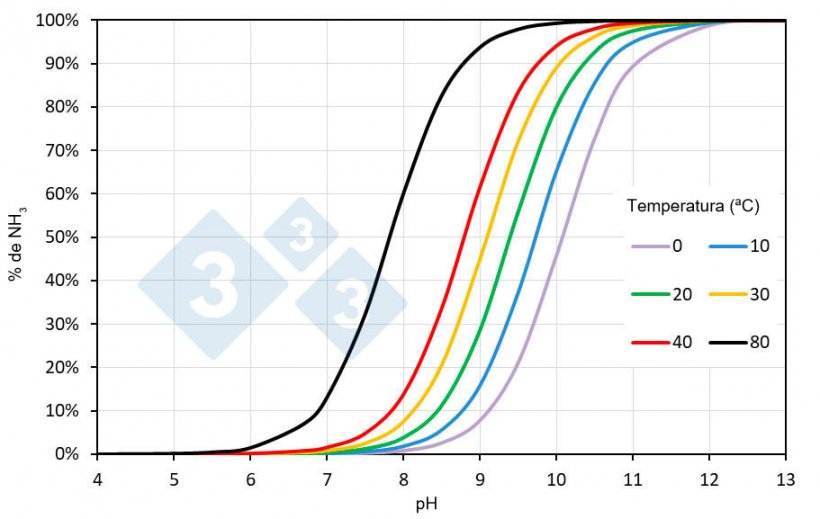
Figura 1. Porcentaje de amoníaco (NH3) en una disolución de nitrógeno amoniacal en agua en función del pH y la temperatura. La salinidad de los purines puede modificar los valores indicados.
El NH3 es un gas, el cual se volatiliza hacia la atmosfera, mientras que la forma ionizada (NH4+) se mantiene soluble. Acidificar los purines, añadiendo un ácido, tiene el interés de desplazar el equilibrio hacia la forma soluble, evitando la formación de amoníaco así como su pérdida por volatilización, o la pérdida del valor fertilizante de los purines.
El total de nitrógeno amoniacal de los purines, suma de NH4+ y de NH3, puede estar comprendido en el rango 1,6 – 7,9 mg N/L, siendo el 55 – 90 % del total del nitrógeno, en función del estado fisiológico de los animales y de la edad de los purines. Por tanto, el valor como fertilizante nitrogenado de los purines está muy relacionado con el contenido de nitrógeno amoniacal, el cual se va perdiendo durante el tiempo de almacenaje en forma de NH3 si no se aplica ninguna técnica para evitarlo.
Se distingue entre el nitrógeno total Kjeldahl, que es la suma del nitrógeno amoniacal y orgánico, y el nitrógeno total, que incluye además nitratos y nitritos. Los purines excretados sólo contienen nitrógeno Kjeldahl pero, en función del tiempo de permanencia en balsas de almacén abierto a la atmosfera, pueden contener también pequeñas concentraciones de nitratos y nitritos.
La acidificación consiste en la adición controlada de un ácido, usualmente sulfúrico, para mantener el pH de los purines entre 5,5 y 6, con lo cual se mantiene prácticamente todo el nitrógeno amoniacal en forma ionizada y se evita la volatilización del amonio. En la Figura 2 se muestra el equipo de dosificación automática de ácido en una granja de cerdos en Dinamarca y en la Figura 3 un equipo de acidificación acoplado al tractor-cuba para evitar la pérdida de amonio durante la fertilización.

Figura 2. Tanque de almacén de ácido en una granja de cerdos en Dinamarca, que acidifica los purines en los fosos de las naves y el almacén exterior de forma controlada y automática.

Figura 3. Equipo acoplado al tractor-cuba para acidificación de purines durante la aplicación agrícola. Foto gentileza de www.vogelsang.info.
La acidificación, aparte de reducir las emisiones de amoníaco, también se ha comprobado que reduce las emisiones de metano a la atmosfera al limitar el medio ácido el crecimiento de los microorganismos anaerobios.
El sistema de acidificación tiene un grado significativo de implantación en Dinamarca, donde el tiempo de almacén es de 9 meses y donde la normativa obliga a cotas elevadas de eficiencia en la fertilización nitrogenada con deyecciones, para lo cual es imprescindible evitar la pérdida de nitrógeno amoniacal, más cuando son necesarios elevados tiempos de almacén. En este sentido, es un proceso adecuado en situación de no excedentes de nitrógeno, para aprovechar todo el potencial fertilizante de los purines y evitar emisiones a la atmosfera.
Acidificar representa un coste de inversión y de operación, el cual puede compensarse en parte por la reducción del consumo de fertilizantes químicos, al aprovechar todo el amonio de los purines.
La acidificación también es necesaria en procesos de concentración térmica, cuando se pretende aprovechar una fuente de energía térmica para evaporar parte del agua de los purines y obtener un producto de menor volumen para facilitar su transporte, sobretodo en situación de excedentes. En este caso, es conveniente aplicar la acidificación a la fracción líquida de los purines después de un proceso de digestión anaerobia, para evitar su volatilización y para reducir o minimizar el contenido de ácidos grasos volátiles, los cuales tienden a volatilizarse a pH ácido, lo cual llevaría a la contaminación por materia orgánica de los vapores de la evaporación o la de su condensado.

¿Qué papel juega la acidificación en situación de no excedentes?) 









